
prof. dr hab. n. med. Adrian Doroszko
Przewlekła niewydolność serca i choroby współistniejące w gabinecie lekarza rodzinnego – jak leczyć, żeby nie zaszkodzić?
Artykuł opublikowany w miesięczniku TERAPIA 2/2021

Optymalna terapia...
przewlekłej niewydolności serca, mimo jasnego i uporządkowanego przekazu wytycznych, jest poważnym wyzwaniem dla lekarza prowadzącego i wymagającym zadaniem dla pacjenta. Poza doborem odpowiednich skojarzeń leków z danych grup, nie należy zapominać o konieczności nieustannego dążenia do dawek docelowych poprzez ciągłą optymalizację terapii. Współistniejące liczne schorzenia przewlekłe często ograniczają możliwość swobodnego doboru leków lub narzucają schematy terapeutyczne, na podstawie odnośnych wytycznych, utrudniając tym samym podjęcie wyważonej decyzji.
Współczesna definicja niewydolności serca – nieoczywista oczywistość
Niewydolność serca (heart failure, HF), zgodnie z obowiązującą definicją (1), stanowi zespół typowych objawów (tj. duszność, obniżenie tolerancji wysiłku, obrzęki kończyn dolnych), którym mogą (lecz nie muszą) towarzyszyć odchylenia w badaniu przedmiotowym (poszerzenie żył szyjnych, trzeszczenia nad płucami, obrzęki obwodowe). Objawy te wynikają z zaburzeń w budowie i/lub czynności serca, prowadząc do spadku jego rzutu i/lub wzrostu ciśnienia wewnątrzsercowego w spoczynku bądź w trakcie wysiłku. Jednak u pacjenta z uprzednio rozpoznaną już HF objawy mogą być nieobecne, jeśli jest optymalnie leczony – wtedy ich brak nie wyklucza rozpoznania niewydolności serca. Warto o tym pamiętać, zważywszy że dokumentacja medyczna chorego często bywa niekompletna, a pacjent może zasięgać opinii u wielu specjalistów. Zgodne z obowiązującymi wytycznymi kryteria rozpoznania i typy przewlekłej niewydolności serca przedstawiono w tabeli 1.
Wstępna diagnostyka przewlekłej niewydolności serca (chronic heart failure, CHF) każdorazowo wymaga ustalenia jej przyczyny. U każdego chorego trzeba dążyć do wyjaśnienia etiologii uszkodzenia serca i wyleczenia potencjalnie odwracalnych
przyczyn – najczęściej:
- należy przeprowadzić szczegółową diagnostykę w kierunku
choroby niedokrwiennej serca; - trzeba wykluczyć istotne wady serca (nabyte lub przeoczone
wrodzone); - należy wykluczyć tachyarytmie jako przyczyny dysfunkcji
lewej komory; - częstą przyczyną jest toksyczne uszkodzenie serca (alkohol,
narkotyki, a także chemioterapia onkologiczna).
Nierzadko etiologii uszkodzenia lewej komory nie daje się jednoznacznie ustalić, szczególnie jeśli spowodowana jest przebytym w przeszłości bezobjawowym lub skąpoobjawowym zapaleniem mięśnia serca.

Farmakoterapia – diabeł tkwi w szczegółach
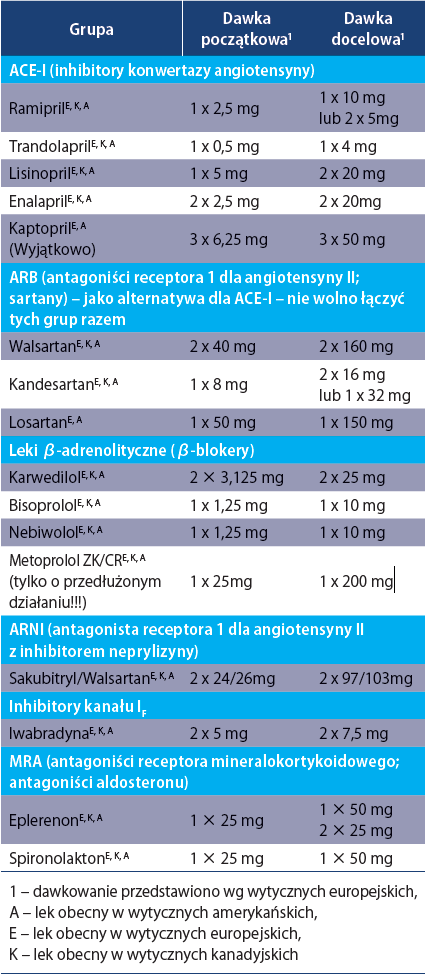
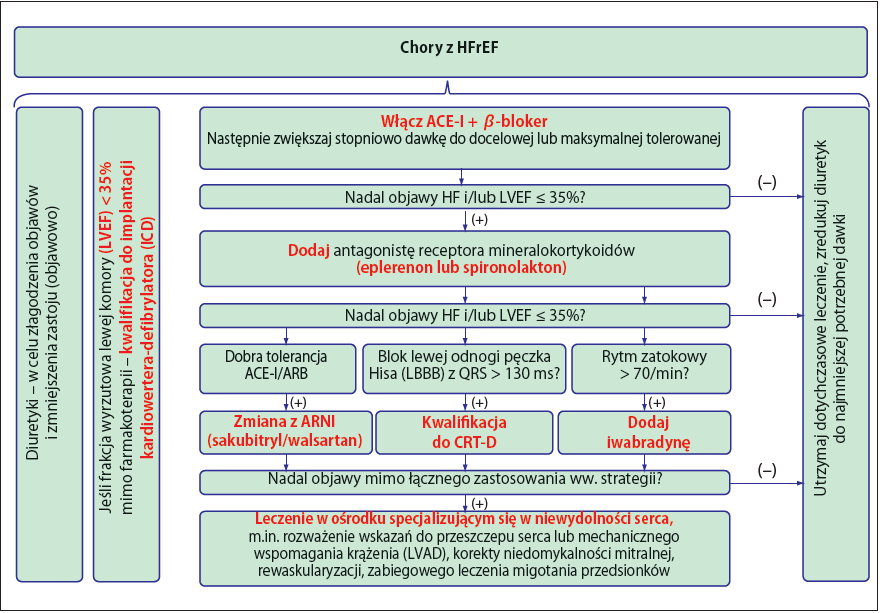
W tabeli 2 zestawiono leki modyfikujące przebieg przewlekłej niewydolności serca z obniżoną frakcją wyrzutową (heart failure with reduced ejection fraction, HFrEF) oraz ich dawkowanie – ich stosowanie zmniejsza śmiertelność oraz częstość dekompensacji chorego i tylko one są rekomendowane w wytycznych europejskich, amerykańskich i kanadyjskich (1–3). Na rycinie 1 przedstawiono z kolei zgodny z obecnie obowiązującymi wytycznymi europejskimi schemat postępowania w HFrEF. Warto zauważyć, że tylko niektóre β-blokery, inhibitory konwertazy angiotensyny (angiotensyn-converting enzyme inhibitors, ACE-I) lub sartany (angiotensin II receptor blockers, ARB) są zalecane w terapii (nie ma jednoznacznie przekonujących dowodów na skuteczność innych leków z danej grupy, a tzw. efekt klasy nie został wystarczająco udokumentowany, by móc zachować pełną dowolność w wyborze leku). Należy zauważyć, że stosowane w terapii nadciśnienia tętniczego ACE-I, jak zofenopril czy perindopril oraz ARB, jak telmisartan, olmesartan, eprosartan czy azilasartan – nie znajdują zastosowania w terapii przewlekłej niewydolności serca, zgodnie z wytycznymi Europejskiego Towarzystwa Kardiologicznego. U każdego pacjenta należy dążyć do stosowania docelowych dawek leków lub maksymalnych tolerowanych, jeśli
osiągniecie tych pierwszych jest niemożliwe. Tylko wtedy mamy wystarczające dowody na redukcję śmiertelności. Diuretyki natomiast są tylko lekami objawowymi – ich stosowanie nie wpływa na śmiertelność i powinny być podawane w najmniejszych skutecznych dawkach, zwiększanych czasowo w okresie dekompensacji. Każdy pacjent z EF < 35% wymaga oceny kardiologicznej pod kątem implantacji kardiowertera-defibrylatora (implantable cardioverter-defibrillator, ICD) jako profilaktyki nagłego zgonu sercowego (sudden cardiac death, SCD) lub układu resynchronizującego z opcją defibrylacji (CRT-D), gdy współistnieje blok lewej odnogi pęczka Hisa (left bundle branch block, LBBB).
Niewydolność serca z zachowaną frakcją wyrzutową (HFpEF) – nierozstrzygnięty problem współczesnej kardiologii
HFpEF (heart failure with preserved ejection fraction) w populacji ogólnej częściej występuje u osób starszych i wówczas zwykle stanowi schyłkowe stadium choroby nadciśnieniowej serca, często współwystępuje z przewlekłą obturacyjną chorobą płuc (POChP) i otyłością, zespołem bezdechu sennego. W rzadszych przypadkach, niekiedy bez wieloletniej historii nadciśnienia tętniczego, choroby płuc czy zaburzeń metabolicznych, HFpEF jest skutkiem kardiomiopatii restrykcyjnej, amyloidozy serca, np. w przebiegu szpiczaka, lub jej objawy rozwijają się w przebiegu zaciskającego zapalenia osierdzia. Poza spadkiem tolerancji wysiłku i dusznością, pierwszą manifestacją może być obrzęk płuc w przebiegu zwyżki ciśnienia tętniczego krwi. Niestety, jak dotąd brak jest jednoznacznych dowodów na redukcję śmiertelności przy stosowaniu terapii jak w HFrEF i obecnie nie ma ustalonego schematu leczenia o znaczeniu rokowniczym. Pojedyncze badania wskazują na spadek częstości dekompensacji i poprawę tolerancji wysiłku w przypadku stosowania tylko niektórych leków. Ich zastosowanie i połączenie w terapii można jednak rozważyć u chorych z HFpEF według wytycznych Kanadyjskiego (Canadian Cardiovascular Society, CCS) i Amerykańskiego (American Heart Association, AHA) Towarzystwa Kardiologicznego, są też wspomniane w wytycznych europejskich. Są to:
- nebiwolol;
- kandesartan;
- eplerenon lub spironolakton;
- diuretyki pętlowe w razie występowania objawów zastoju.
Aktualnie brak jest dowodów na występowanie efektu klasy dla ww. leków, a kilka badań z innymi przedstawicielami tych grup nie wykazało żadnych korzyści z ich stosowania.
Niewydolność serca a choroby współistniejące ‒ czy na pewno robimy wszystko, co możliwe, by poprawić rokowanie?
Cukrzyca typu 2
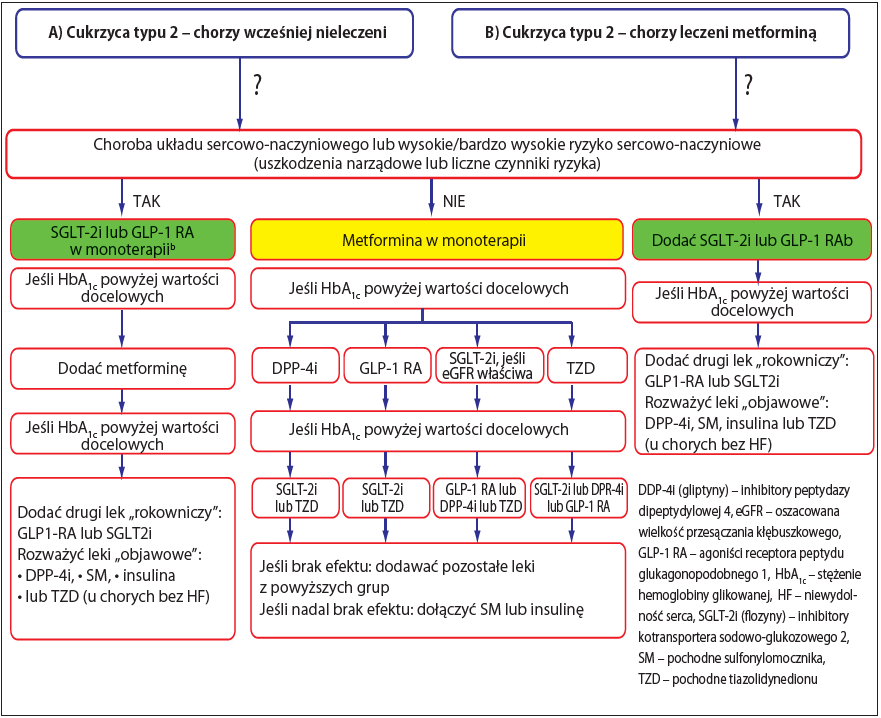
Wytyczne European Society of Cardiology (ESC) z 2019 r. (4) dotyczące cukrzycy i stanu przedcukrzycowego jasno precyzują algorytm terapii u chorych ze współwystępującymi chorobami układu sercowo-naczyniowego, w tym przewlekłej niewydolności serca (ryc. 2). Warto zauważyć, że preferowane jest stosowanie leków poprawiających rokowanie, czyli o udowodnionej skuteczności w redukcji zdarzeń sercowo-naczyniowych. W związku z tym metforminę w monoterapii preferuje się u chorych rozpoczynających leczenie cukrzycy, gdy jeszcze nie współistnieją liczne powikłania i zaawansowane choroby układu sercowo-naczyniowego. Do niej z kolei należy dołączyć inhibitor kotransportera sodowo-glukozowego 2 (sodiumglucose co-transporter 2, SGLT-2; flozyna) lub agonistę receptora peptydu glukagonopodobnego 1 (glucagon-like peptide 1, GLP-1), m.in. liraglutyd, eksenatyd, semaglutyd, jako leki o znaczeniu rokowniczym, które zyskują na znaczeniu w miarę progresji powikłań. Od nich powinno się rozpoczynać terapię u chorych z bardzo wysokim ryzykiem lub po przebytych incydentach sercowo-naczyniowych. Niezależne badania DAPA-HF i wcześniejsze EMPA-REG OUTCOME oraz EMPEROR-Reduced (5) potwierdziły skuteczność dapagliflozyny i empagliflozyny w spowalnianiu progresji niewydolności serca, redukcji objawów i śmiertelności sercowo-naczyniowej. Co ciekawe, ryzyko pogorszenia niewydolności serca lub zgonu było niższe u osób przyjmujących flozynę w porównaniu ze stosującymi placebo, niezależnie od współwystępowania cukrzycy (6).
Warto zauważyć, że pochodne sulfonylomocznika są obecnie lekami ostatniego wyboru – korygują bowiem glikemię przy braku dowodów na redukcję śmiertelności i zdarzeń sercowo-naczyniowych.
Nadciśnienie tętnicze (6)
Optymalizacja farmakoterapii schorzeń sercowo-naczyniowych powinna opierać się na dążeniu do stosowania leków o znaczeniu rokowniczym (tj. zmniejszających częstość zdarzeń sercowo-naczyniowych i/lub śmiertelności) w dawkach o udowodnionej skuteczności. Pozostałe leki (o znaczeniu objawowym) należy stosować w miarę potrzeby, w dostosowanej dawce. Dążąc do docelowych dawek leków o działaniu rokowniczym, należy redukować lub odstawić pozostałe leki hipotensyjne, niemające wpływu lub mogące pogorszyć przebieg niewydolności serca.
Spośród dihydropirydynowych antagonistów wapnia jedynie amlodypina jest uważana za lek bezpieczny i może być stosowana, jeśli mimo osiągniecia docelowych dawek leków o znaczeniu rokowniczym utrzymuje się podwyższone ciśnienie tętnicze krwi. Należy odstawić i unikać leków o działaniu α-adrenolitycznym (m.in. doksazosyna, tamsulozyna) ze względu na badania wskazujące na ich negatywny wpływ na kontrolę objawów i śmiertelność. Bezwzględnie przeciwwskazane są niesteroidowe leki przeciwzapalne (NLPZ), pioglitazon, werapamil i diltiazem – zwiększają częstość dekompensacji i ryzyko zgonu pacjenta.
Przewlekły zespół wieńcowy (7,8)
Należy dążyć do optymalizacji kontroli czynników ryzyka i przebiegu chorób towarzyszących, a w ich terapii stosować te leki, które mają udowodnione dodatkowo korzystne oddziaływanie na przebieg współistniejącej HF. W przypadku współistniejącej choroby niedokrwiennej serca należy włączyć dodatkowo kwas acetylosalicylowy 75 mg/d lub klopidogrel 75 mg/d oraz statynę. Niewydolność serca o etiologii innej niż niedokrwienna nie wymaga stosowania tych leków, gdyż nie poprawiają one rokowania.
Zaburzenia gospodarki lipidowej
Terapia hipolipemizująca znajduje uzasadnienie w leczeniu niewydolności serca, ale tylko o etiologii niedokrwiennej, kiedy to wskutek choroby wieńcowej czy przebytego zawału dochodzi do spadku frakcji wyrzutowej. Jej znaczenie polega głównie na zapobieganiu kolejnym ostrym zespołom wieńcowym prowadzącym do progresji dysfunkcji skurczowej lewej komory. Pacjent taki przypisany jest do grupy bardzo wysokiego ryzyka sercowo-naczyniowego i dlatego zgodnie z wytycznymi ESC z 2019 r. (8) należy dążyć do uzyskania docelowych wartości LDL cholesterolu poniżej 55 mg/dl (1,4 mM). Jeśli terapia samą statyną okazuje się nieskuteczna mimo eskalacji dawki, trzeba dołączyć do niej ezetimib, a w razie dalszego niepowodzenia terapeutycznego, należy pacjenta skierować do poradni zaburzeń lipidowych celem kwalifikacji do leczenia inhibitorami PCSK9 (proprotein convertase subtilisin/kexin 9). Warto zauważyć, że w przypadku niewydolności serca o etiologii innej niż niedokrwienna nie ma dowodów na skuteczność statyn w poprawie rokowania, o ile tylko nie istnieją inne schorzenia współistniejące wymagające jej stosowania.
Dlatego rutynowe włączanie statyn u pacjenta z nie-niedokrwienną etiologią niewydolności serca przy braku innych wskazań do ich stosowania jest bezzasadne.
POChP, astma i objawy niepożądane terapii ze strony układu oddechowego
W ostatnich latach obserwujemy znaczną liberalizację przeciwwskazań do stosowania leków β-adrenolitycznych u osób ze współistniejącymi przewlekłymi chorobami układu oddechowego oraz rozszerzenie ich wskazań. Opisywane w starszej literaturze ryzyko nasilenia obturacji okazuje się w praktyce nie tak częste, jak do tej pory uważano. Natomiast wykazanie, że terapia β-blokerami może zmniejszać częstość zaostrzeń POChP spowodowała, iż leki te nie są już przeciwwskazane u osób z tym schorzeniem. Ponadto nie są one już bezwzględnie przeciwwskazane w przypadku astmy oskrzelowej – w razie istnienia kardiologicznych wskazań klinicznych do ich stosowania u pacjentów z dobrze kontrolowaną astmą, należy podjąć próbę takiej terapii, preferując leki kardioselektywne. Zatem współistniejące POChP lub dobrze kontrolowana astma nie powinny być przeszkodą we wdrożeniu optymalnej terapii niewydolności serca, uwzględniającej β-bloker, przy czym rozsądny wydaje się wybór nebiwololu lub bisoprololu.
Omawiając terapię przewlekłej niewydolności serca i schorzenia układu oddechowego, warto także wspomnieć, że przewlekły kaszel, często przypisywany stosowanym ACE-I, wbrew pozorom nierzadko jest skutkiem innej współistniejącej patologii, jak np. choroba refluksowa przełyku, przewlekle zapalenie zatok czy infekcje atypowe. Jedną z przyczyn może być oczywiście wzrost stężenia bradykininy w płucnym łożysku naczyniowym wskutek zmniejszenia jej rozkładu przez zablokowaną konwertazę angiotensyny, jednak nie jest to zjawisko częste i zwykle pojawia się na początku, a nie po wielu miesiącach/latach terapii inhibitorami ACE. Warto zauważyć, że wzrost stężenia bradykininy, jeśli tylko nie wiąże się z wystąpieniem kaszlu, jest zjawiskiem bardzo korzystnym, wywierając pozytywne przeciwzapalne działanie na śródbłonek naczyniowy, zwiększając biodostępność tlenku azotu i obniżając ciśnienie w płucnym łożysku naczyniowym. Wszystkie te elementy determinują wyższość ACE-I nad ARB, która uwidacznia się szczególnie w sytuacji terapii zaawansowanych schorzeń układu sercowo-naczyniowego (9) – im pacjent jest bardziej chory, tym bardziej widoczna jest ta przewaga. Pochopne odstawianie leków z tej grupy, bez przeprowadzenia wnikliwej diagnostyki różnicowej kaszlu, jest więc błędem, gdyż pozbawia chorego szans na stosowanie terapii przedłużającej życie. W sytuacji potwierdzonego związku przyczynowo-skutkowego między stosowaniem ACE-I a występowaniem kaszlu, w przypadku współistniejącej niewydolności serca należy zastosować jeden z trzech dozwolonych ARB (losartan, kandesartan lub walsartan), a w sytuacji zaawansowanej niewydolności serca zamienić na antagonistę receptora 1 dla angiotensyny II z inhibitorem neprylizyny (angiotensin receptor-neprilysin inhibitor, ARNI): sakubitryl z walsartanem, po zachowaniu optymalnie 36-godzinnej przerwy między ostatnią dawką ACE-I a pierwszą dawką ARNI. Podyktowane jest to podwyższonym ryzykiem wystąpienia obrzęku naczynioruchowego przy równoległym zastosowaniu ACE-I z sakubitrylem, i właśnie ta negatywna interakcja stała się także powodem dołączenia w omawianym złożeniu sartanu do sakubitrylu, zamiast ACE-I.
Przewlekła choroba nerek (10,11)
Powiązania przewlekłej niewydolności serca z przewlekłą chorobą nerek (chronic kidney disease, CKD) są wielokierunkowe i mogą wynikać zarówno z zaawansowanej miażdżycy w obu łożyskach naczyniowych, jak i stanowić wyraz powikłań narządowych nadciśnienia tętniczego, wtedy jednak częściej niewydolności nerek towarzyszy HFpEF, a skrajną manifestacją choroby może być nawracający obrzęk płuc w przebiegu zwyżek ciśnienia. Inną sytuacją, występującą częściej w przebiegu zaawansowanej niewydolności serca jest przewlekły zespól sercowo-nerkowy, kiedy to znaczny spadek pojemności minutowej uszkodzonego mięśnia sercowego połączony z zastojem żylnym skutkuje upośledzoną perfuzją nerek i spadkiem filtracji kłębuszkowej. Rozróżnienie tych patomechanizmów jest niezmiernie istotne, umożliwia bowiem optymalizację terapii prowadzącą do stabilizacji funkcji nerek i zmniejszenia objawów niewydolności serca.
W przypadku uszkodzenia przez nadciśnienie tętnicze nerek i serca (najczęściej HFpEF), wskazana jest optymalizacja jego kontroli (12), uzyskiwana najczęściej przez połączenie ACE-I z diuretykiem (tiazydopodobnym przełączanym na pętlowy przy spadku eGFR < 30 ml/min) i antagonistą wapnia (amlodypiną – neutralną z perspektywy niewydolności serca). Spośród leków β-adrenolitycznych udowodniony pozytywny wpływ na funkcję nerek u chorych z HF i CKD ma karwedilol (13). Optymalizacja terapii spowalnia progresję przewlekłej choroby nerek (14) oraz ryzyko nawracającego obrzęku płuc. Warto zauważyć, że ACE-I i sartany są lekami o udowodnionym działaniu nefroprotekcyjnym i ich stosowanie spowalnia progresję przewlekłej choroby nerek. Obserwowany nieznaczny wzrost stężenia kreatyniny (o ok. 30% w stosunku do wartości wyjściowych) z towarzyszącym spadkiem filtracji kłębuszkowej jest akceptowalny i wynika ze spadku ciśnienia filtracji w kłębuszkach, a więc jest wyrazem działania ochronnego blokerów układu renina-angiotensyna-aldosteron (RAA). Częstym błędem jest niewłączanie lub odstawianie ACE-I czy sartanów u chorych, u których obserwowane są obniżone wartości eGFR, co skutkuje pozbawieniem ich szans na leczenie nefro- i kardioprotekcyjne jednocześnie. Obowiązujące wytyczne leczenia przewlekłej niewydolności serca zalecają zachowanie ostrożności i redukcję dawki ACE-I lub sartanu oraz skierowanie pacjenta do nefrologa dopiero przy wzroście stężenia kreatyniny w surowicy > 2,5 mg/dl (221 μM) lub spadku eGFR < 30 ml/min/1,73 m2. Oczywiście, bezwzględnie przeciwwskazane jest łączenie ACE-I z ARB, bowiem zwiększa ono częstość występowania schyłkowej niewydolności nerek przy braku przekonującej dodatkowej korzyści w terapii niewydolności serca czy nadciśnienia tętniczego.
Choroba naczyniowa mózgu (15,16)
Wobec wielochorobowości pacjenta i liczby przyjmowanych leków, a także ograniczonej sprawności psychoruchowej po przebytym udarze mózgu racjonalne jest maksymalne upraszczanie schematów terapeutycznych, preferencyjnie co 12 godz., z pominięciem konieczności przyjmowania leków w środku dnia. Rozsądne jest także minimalizowanie liczby przyjmowanych tabletek poprzez stosowanie preparatów
złożonych zawierających kilka substancji czynnych w jednej tabletce. Taka strategia zwiększa znacząco compliance ze strony pacjenta poprzez łatwość stosowania się do zaleceń, minimalizację ryzyka pomyłek przy przygotowywaniu porcji leków. Zmniejsza to także obawy chorego dotyczące możliwych działań niepożądanych, wielości interakcji lub poczucia ciężkiej choroby wobec konieczności przyjmowania niekiedy kilkunastu tabletek dziennie. Dostępne wielolekowe połączenia złożone w jednej tabletce mogą więc być stosowane nie tylko w terapii nadciśnienia tętniczego, ale i współistniejącego naczyniopochodnego uszkodzenia mózgu. Preparaty zawierające w złożeniu dwa lub docelowo trzy spośród następujących grup leków: diuretyk tiazydopodobny, ACE-I, antagonista wapnia, a dodatkowo statyna i klopidogrel lub kwas acetylosalicylowy wydają się optymalną opcją łączącą poprawność merytoryczną terapii pacjenta z naczyniową chorobą mózgu (17) i nadciśnieniem tętniczym (18), przy współistniejącej niewydolności serca.
Dekompensacja – czerwona flaga w przebiegu choroby czy żółta kartka dla lekarza prowadzącego?
Dekompensacja niewydolności serca stanowi nie tylko doraźne pogorszenie kliniczne, lecz jest również wyrazem progresji choroby, a jej skutki negatywnie przekładają się na rokowanie odległe. Dlatego należy kłaść szczególny nacisk, aby u osób z zaawansowaną HF prowadzonych ambulatoryjnie nawet niewielkie pogorszenie kontroli objawów skutkowało natychmiastową optymalizacją terapii celem uniknięcia dekompensacji. Każdorazowo należy dążyć do zidentyfikowania i wyeliminowania potencjalnych przyczyn dekompensacji. Biorąc je pod uwagę, należy podjąć decyzję o hospitalizacji lub optymalizacji leczenia w trybie ambulatoryjnym. Są to najczęściej:
- Ostry zespól wieńcowy, w tym przebyty ambulatoryjnie (nieświadomie) ‒ zarówno ostra faza zawału mięśnia sercowego, jak i spadek frakcji wyrzutowej będący jego skutkiem są czynnikami prowadzącymi do dekompensacji oraz pogorszenia funkcjonowania pacjenta, oceniając go w skali NYHA.
- Tachyarytmie (migotanie przedsionków, komorowe zaburzenia rytmu) ‒ mogą być subiektywnie nieodczuwalne, dlatego każdorazowo przed wizytą lekarską spowodowaną pogorszeniem tolerancji wysiłku chory powinien mieć wykonane
spoczynkowe EKG. Komorowe zaburzenia rytmu przy współistniejącej strukturalnej chorobie serca niosą bezpośrednie ryzyko nagłego zgonu sercowego, które proporcjonalnie wzrasta wraz ze spadkiem frakcji wyrzutowej. Tachyarytmie, jak np. migotanie przedsionków przebiegające z szybką czynnością komór, mogą wyindukować ostry zespół wieńcowy u pacjenta ze zmniejszoną rezerwą wieńcową, a jeśli trwają dłużej – kardiomiopatię tachyarytmiczną. W tej sytuacji ważne jest rozróżnienie, czy tachyarytmia pojawiła się u osoby z już istniejącą niewydolnością serca i rozstrzenią lewej komory, czy też jest ona pierwotną przyczyną rozwoju HF. Jeśli rozstrzeń lewej komory i dysfunkcja skurczowa pojawiły się wyłącznie wskutek tachyarytmii, jest to scenariusz relatywnie korzystny, gdyż wyleczenie zaburzeń rytmu i optymalizacja terapii mogą odwrócić przebudowę mięśnia sercowego i spowodować normalizację funkcji lewej komory. - Nieoptymalna kontrola ciśnienia tętniczego oraz nieregularne stosowanie leków lub samowolna modyfikacja dawkowania – z taką sytuacją szczególnie często mamy do czynienia u pacjentów z HFpEF przyjmowanych do szpitala z objawami obrzęku płuc w przebiegu zwyżki ciśnienia tętniczego.
- Infekcje (zapalenie płuc, zakażenie układu moczowego [ZUM], sepsa), zaostrzenie POChP – u osób starszych ich rozpoznanie bez badań dodatkowych może być niemożliwe, w związku z czym łatwo je przeoczyć, co może kosztować życie pacjenta.
- Złe stosowanie diuretyków, nieoptymalne spożycie płynów lub soli kuchennej ‒ należy uświadomić choremu, że szybki systematyczny przyrost masy ciała „z dnia na dzień” najprawdopodobniej oznacza retencję płynów i wymaga zmiany dawkowania pewnych leków, a zatem pilnej wizyty u lekarza prowadzącego. Należy starać się uświadomić choremu znaczenie jego „suchej masy ciała” (podobnie jak u osób dializowanych – zmierzonej w momencie optymalnego stanu nawodnienia organizmu, przy braku objawów dekompensacji) i przekonać, że jej utrzymanie jest kluczowe z punktu widzenia optymalnego leczenia i samopoczucia. Świadomi pacjenci w pewnym ograniczonym zakresie mogą samodzielnie modyfikować dawkowanie diuretyków, pamiętając jednak o konieczności regularnego sprawdzania funkcji nerek i elektrolitów w surowicy. Osobom z zaawansowaną HF należy zalecić restrykcję spożycia płynów – ok. 1,5 l dziennie oraz znacznie ograniczyć spożycie soli kuchennej.
- Bradyarytmie/bradykardia – subiektywnie pacjent może zgłaszać jedynie spadek tolerancji wysiłku; pomiary ciśnienia oraz tętna powinny być integralnym elementem każdej wizyty, a także winny być regularnie monitorowane samodzielnie przez chorego lub jego najbliższych i ewidencjonowane w dzienniczku samokontroli. Znaczna bradykardia pojawiająca się np. w przebiegu bloku przedsionkowo-komorowego II lub III stopnia jest bezpośrednim stanem zagrożenia życia i wymaga pilnej hospitalizacji celem kwalifikacji do implantacji stymulatora. W innych sytuacjach (migotanie przedsionków z wolną czynnością komór, nasilona objawowa bradykardia w przebiegu zespołu tachy-brady lub stała bradykardia zatokowa) przy zachowanej pełnej stabilności hemodynamicznej pacjenta wymagają w pierwszej kolejności weryfikacji adekwatności dawkowania leków o działaniu chronotropowo ujemnym (β-blokerów, iwabradyny lub digoksyny) i po wykluczeniu ww. wtórnej przyczyny, rozważenia wskazań do implantacji układu stymulującego.
- Stosowanie leków przeciwwskazanych w niewydolności serca (m.in. NLPZ, pioglitazon w leczeniu cukrzycy, diltiazem, werapamil, kardiotoksyczna chemioterapia, steroidoterapia, nadużywanie wziewnych β-mimetyków, teofilina – lek o znaczeniu niemal historycznym, nadal często i błędnie stosowany w POChP). Należy wyczulić pacjentów na konieczność unikania samowolnego decydowania o przyjmowaniu leków, zwłaszcza przeciwzapalnych, a także o konieczności informowania lekarzy innych specjalności o współistniejącej HF, ograniczającej w pewnym stopniu swobodę terapii schorzeń współistniejących.
- Zatorowość płucna – jest jedną z łatwiejszych do przeoczenia chorób układu sercowo-naczyniowego, szczególnie u pacjenta z nakładającymi się innymi schorzeniami mogącymi powodować duszność i mniejszą tolerancję wysiłku fizycznego. Jej symptomatologia może być nieadekwatna do rozległości zamknięcia płucnego łożyska tętniczego przez skrzeplinę, powodując niedoszacowanie ciężkości stanu klinicznego i ryzyka zgonu. Nieuwzględnienie jej w diagnostyce różnicowej, skutkujące nieprzeprowadzeniem dedykowanych badań (oznaczenie d-dimeru w celu wykluczenia przy małym prawdopodobieństwie, echokardiografia w połączeniu z angio-TK tętnic płucnych w szpitalnych oddziałach ratunkowych przy wysokim prawdopodobieństwie, może kosztować życie pacjenta przy pozostawieniu go bez leczenia przeciwkrzepliwego. Mała aktywność fizyczna, obrzęki kończyn dolnych, a zwłaszcza unieruchomienie w łóżku w okresie dekompensacji są istotnymi czynnikami sprzyjającymi zatorowości płucnej. Mając to na uwadze, należy dokładać szczególnej staranności w identyfikacji jej czynników ryzyka i wdrażać odpowiednią profilaktykę, zgodnie z właściwymi wytycznymi.
- Zaburzenia hormonalne/metaboliczne: dysfunkcja tarczycy, nieuregulowana cukrzyca, okres ciąży i połogu). Zaburzenia funkcji tarczycy są istotnym elementem pogarszającym przebieg większości chorób układu sercowo-naczyniowego. Nadczynność tarczycy, poprzez znaczące zwiększenie tempa przemiany materii, tkankowego zapotrzebowania na tlen, aktywacji układu współczulnego zwiększającej obciążenie serca i promującej tachyarytmie, jest istotnym czynnikiem sprzyjającym dekompensacji. Z kolei niedoczynność tarczycy, poprzez deficyt hormonów o działaniu kardiotropowo dodatnim, współistniejącej tendencji do retencji płynów, zwiększającej obciążenie następcze serca, także sprzyja dekompensacji. Dlatego okresowy skrining pod kątem dysfunkcji tarczycy, jak i regularna kontrola efektywności leczenia w przypadku rozpoznanej dysfunkcji są kluczowe dla utrzymania homeostazy układu sercowo-naczyniowego i profilaktyki dekompensacji niewydolności serca.
Zła kontrola cukrzycy lub stosowanie leków o działaniu niekorzystnymw niewydolności serca (pioglitazon), niestosowanie leków o działaniu rokowniczym (zwłaszcza flozyn), mimo braku przeciwwskazań, zwiększają zarówno ryzyko dekompensacji, jak i zdarzeń sercowo-naczyniowych (zawał serca, udar mózgu). Optymalizacja terapii cukrzycy powinna polegać nie tylko na uzyskaniu zadowalającej kontroli glikemii, lecz także osiągnieciu tego celu, opierając się na preferowanych w niewydolności serca połączeniach leków, co omówiono już we wcześniejszej części niniejszego opracowania.
Ciąża, poród i połóg są okresami większego obciążenia hemodynamicznego serca, na co nakładają się zmiany hormonalne dodatkowo zwiększające ryzyko dekompensacji HF. Ciąża pacjentki z uprzednio rozpoznaną niewydolnością serca z założenia traktowana jest jako wysokiego ryzyka i bezwzględnie wymaga ścisłego nadzoru kardiologicznego oraz ginekologicznego z uwagi na ryzyko progresji choroby stwarzające zagrożenie życia matki i dziecka. Jednocześnie poważnym problemem jest indukowana ciążą niewydolność serca u osoby uprzednio zdrowej, czyli tzw. kardiomiopatia połogowa. Jej pierwsze objawy (tj. spadek tolerancji wysiłku fizycznego, duszność wysiłkowa, niewielkie obrzęki podudzi, uczucie kołatania serca) mogą być trudne do uchwycenia bez badań specjalistycznych, zwłaszcza wobec ryzyka pomylenia ich ze zmianami typowymi dla zaawansowanej ciąży. Nierozpoznana lub niewłaściwie rozpoznana kardiomiopatia połogowa stanowi ogromne zagrożenie, natomiast w przypadku odpowiednio wczesnego rozpoznania i optymalnego leczenia wzrastają szanse na urodzenie dziecka i przeżycie matki. Warto zauważyć, że jest ona, obok kardiomiopatii tachyarytmicznej i toksycznej, kolejną z potencjalnie odwracalnych przyczyn niewydolności serca. Fakt jej przebycia stanowi natomiast przeciwwskazanie do kolejnej ciąży ze względu na duże ryzyko nawrotu i dramatycznego przebiegu.
- Udar mózgu – w tym przypadku dekompensacja niewydolności serca może wynikać z kilku przyczyn. Ciężka ogólnoustrojowa choroba, aktywacja układu współczulnego, możliwe powikłania udaru obejmujące ciężkie infekcje czy wtórną do unieruchomienia żylną chorobę zakrzepowo-zatorową same w sobie znacząco zwiększają prawdopodobieństwo wystąpienia dekompensacji współistniejącej niewydolności serca. Jej prawdopodobieństwo wzrasta znacząco wskutek nieadekwatnej płynoterapii dożylnej w okresie nagłej hospitalizacji w oddziale neurologicznym lub internistycznym, często połączonej z całkowitą zmianą schematu stosowanych leków. Skupiając się na leczeniu udaru i/lub normalizacji ciśnienia tętniczego, marginalizowane lub pomijane bywa rozpoznanie współistniejącej HF, skutkując dekompensacją wraz z licznymi powikłaniami pogarszającymi rokowanie. Dlatego warto również zweryfikować schematy terapeutyczne proponowane na kartach informacyjnych pacjentów wypisywanych po przebytym udarze mózgu, podobnie jak i po hospitalizacji z powodu innych ciężkich schorzeń przewlekłych. Koniecznie należy zwrócić uwagę, czy w leczeniu uwzględniono wszystkie leki o znaczeniu rokowniczym, wskazane do stosowania na danym etapie niewydolności serca.
Istotnym, ale wbrew pozorom najczęściej zapominanym ambulatoryjnie krokiem jest optymalizacja dawkowania. Pamiętać należy, że w terapii HF, obok doboru optymalnego połączenia leków, równie ważnym zadaniem jest dążenie do dawek docelowych, czyli maksymalnych zalecanych lub maksymalnych tolerowanych przez pacjenta, gdyż tylko w takim przypadku mamy dowody na skuteczność terapii i poprawę rokowania. Chory wypisywany ze szpitala, szczególnie po przebytej dekompensacji, ma zazwyczaj wdrożone leczenie wstępne, będące wówczas maksymalnym tolerowanym. Jednakże w miarę postępującej stabilizacji po wypisie należy sukcesywnie podczas każdej kolejnej wizyty rewidować stosowane leczenie, oceniając możliwość osiągnięcia docelowego dawkowania.
Podsumowanie
Optymalna terapia przewlekłej niewydolności serca, mimo jasnego i uporządkowanego przekazu wytycznych, jest wymagającym zadaniem dla pacjenta i pozostaje poważnym wyzwaniem dla lekarza prowadzącego. Poza doborem odpowiednich skojarzeń leków z danych grup, nie należy zapominać o konieczności nieustannego dążenia do dawek docelowych poprzez ciągłą optymalizację terapii, kierując się przy tym objawami zgłaszanymi przez chorego, a także regularną samokontrolą ciśnienia, tętna i masy ciała. Dekompensacja HF, nawet o łagodnym, niewymagającym hospitalizacji przebiegu, poza optymalizacją dawkowania leków, wymaga każdorazowo wnikliwej analizy jej potencjalnych przyczyn, bowiem ich przeoczenie może skutkować śmiercią chorego. Pamiętając, że frakcja wyrzutowa lewej komory jest jednym z najsilniejszych predyktorów zgonu, a zarazem łatwo dostępnym do zmierzenia parametrem, należy chorego regularnie kierować do oceny echokardiograficznej. Nie wolno przeoczyć momentu jej spadku poniżej 35%, kiedy to znacząco wzrasta ryzyko nagłego zgonu sercowego w mechanizmie migotania komór, a w związku z tym należy chorego skierować do kardiologa celem implantacji kardiowertera-defibrylatora (ICD).
Należy pamiętać, że jeśli mimo stosowanego połączenia trzech podstawowych grup leków o znaczeniu rokowniczym w optymalnych dawkach (czyli β-blokera, ACE-I/sartanu i MRA – eplerenonu lub spironolaktonu) objawy nadal utrzymują się, to należy rozważyć optymalizację terapii poprzez zamianę ACE-I na ARNI (sakubitryl/walsartan) z zachowaniem 36-godzinnej przerwy między ich podaniem, zastosować iwabradynę, jeśli częstość rytmu zatokowego przekracza 70/min mimo maksymalnej lub docelowej dawki β-blokera, a szczególnie w przypadku współistniejącej cukrzycy – dołączyć, przy braku przeciwwskazań, flozynę.
Niezależnie od farmakoterapii, nie wolno zapominać o powszechnie dostępnych opcjach leczenia pozafarmakologicznego poprawiającego rokowanie. Objawowych pacjentów ze współistniejącym LBBB należy konsultować kardiologicznie pod kątem kwalifikacji do implantacji układu resynchronizującego (CRT; często w ramach implantacji kardiowertera-defibrylatora jako profilaktyki pierwotnej nagłego zgonu sercowego, a także w miarę progresji choroby jako rozbudowa uprzednio implantowanego ICD do układu resynchronizującego – CRT-D). Natomiast pacjentów, u których pojawia się istotna niedomykalność zastawki mitralnej, należy kierować do dokładnej oceny echokardiograficznej pod kątem jej mechanizmu celem kwalifikacji do mało inwazyjnej metody leczenia, jaką jest założenie zapinki MitraClip podczas przezskórnej interwencji wykonywanej w pracowni hemodynamiki.
Osoba z postępującą HF, po wyczerpaniu powyższych opcji terapeutycznych, powinna być oceniona podczas hospitalizacji przez kardiogrupę (heart team) pod kątem kwalifikacji do dalszych możliwych działań terapeutycznych, takich jak transplantacja serca lub mechaniczne wspomaganie krążenia (left ventricular assist device, LVAD). Kluczową rolą lekarza koordynującego na co dzień ambulatoryjne leczenie jest więc wychwycenie momentów progresji choroby (wyniki badań) i pogorszenia klinicznego (objawy). Dzięki temu – mając świadomość dostępnych dalszych opcji terapeutycznych – nie pozbawi pacjenta szans na skorzystanie z nich, biernie patrząc na postęp choroby w jej terminalnym stadium, lecz skieruje go do specjalistycznego ośrodka celem precyzyjnej kwalifikacji i wdrożenia konkretnej, spersonalizowanej strategii przedłużającej życie.
Piśmiennictwo:
- Ponikowski P., Voors A.A., Anker S.D. i wsp.: 2016 ESC Guidelines
for the diagnosis and treatment of acute and chronic heart failure: The Task Force for the diagnosis and treatment of acute and chronic heart failure of the European Society of Cardiology (ESC). Developed with the special contribution of
the Heart Failure Association (HFA) of the ESC. Eur J Heart Fail 2016, 18(8): 891–975. - Yancy C.W., Jessup M., Bozkurt B. i wsp.: 2017 ACC/AHA/HFSA Focused Update of the 2013 ACCF/AHA Guideline for the Management of Heart Failure: A Report of the American College of Cardiology/American Heart Association Task Force on Clinical Practice Guidelines and the Heart Failure Society of America. J Am Coll Cardiol 2017, 70(6): 776–803.
- Ezekowitz J.A., O’Meara E., McDonald M.A. i wsp.: 2017 Comprehensive Update of the Canadian Cardiovascular Society Guidelines for the Management of Heart Failure. Can J Cardiol 2017, 33(11): 1342-1433.
- Cosentino F., Grant P.J., Aboyans V. i wsp.: 2019 ESC Guidelines on diabetes, pre-diabetes, and cardiovascular diseases developed in collaboration with the EASD. Eur Heart J 2020, 41(2): 255‒323.
- Packer M., Anker S.D., Butler J. i wsp.: Effect of Empagliflozin on the Clinical Stability of Patients with Heart Failure and a Reduced Ejection Fraction: The EMPEROR-Reduced Trial. Circulation 2020 Oct 21. Doi: 10.1161/CIRCULATIONAHA.120.051783.
- McMurray J.J.V., DeMets D.L., Inzucchi S.E. i wsp.: DAPA-HF Committees and Investigators. A trial to evaluate the effect of the sodium-glucose co-transporter 2 inhibitor dapagliflozin on morbidity and ortality in patients with heart failure and reduced left ventricular ejection fraction (DAPA-HF). Eur J Heart Fail 2019 May, 21(5): 665–675.
- Knuuti J., Wijns W., Antti Saraste A. i wsp.: 2019 ESC Guidelines for the diagnosis and management of chronic coronary syndromes The Task Force for the diagnosis and management of chronic coronary syndromes of the European Society of Cardiology (ESC). Eur Heart J 2020 Jan 14, 41(3): 407‒477.
- Khan N.A., Rabkin S.W., Zhao Y. i wsp.: Effect of Lowering Diastolic Pressure in Patients With and Without Cardiovascular Disease: Analysis of the SPRINT (Systolic Blood Pressure Intervention Trial). Hypertension 2018 May, 71(5): 840–847.
- Epstein B.J., Gums J.G.: Angiotensin receptor blockers versus ACE inhibitors: prevention of death and myocardial infarction in high-risk populations. Ann Pharmacotherapy 2005, 39: 470–480.
- Safian R.D., Textor S.C.: Renal-artery stenosis. N Engl J Med 2001, 344(6): 431–442.
- Bansal N., McCulloch C.E., Lin F. i wsp.; CRIC Study Investigators: Different components of blood pressure are associated with increased risk of atherosclerotic cardiovascular disease versus heart failure in advanced chronic kidney disease. Kidney Int 2016 Dec, 90(6): 1348–1356.
- Chang A.R., Lóser M., Malhotra R., Appel L.J.: Blood Pressure Goals in Patients with CKD: A Review of Evidence and Guidelines. Clin J Am Soc Nephrol 2019, 14(1): 161–169.
- Bakris G.L., Hart P., Ritz E.: Beta blockers in the management of chronic kidney disease. Kidney Int 2006, 70: 1905–1913.
- Aboyans V., Ricco J.B., Bartelink M.L. i wsp.: The 2017 ESC Guidelines on the Diagnosis and Treatment of Peripheral Arterial Diseases, in collaboration with the Europe-an Society for Vascular Surgery (ESVS): Document cove-ring atherosclerotic disease of extracranial carotid andvertebral, mesenteric, renal, upper and lower extremity arteries. Endorsed by: the European Stroke Organization (ESO). The Task Force for the Diagnosis and Treatment of Peripheral Arterial Diseases of the European Society of Cardiology (ESC) and of the European Society for Vascular Surgery (ESVS). Eur Heart J 2018, 39(9): 763–816.
- Katsanos A.H., Pikilidou M., Kargiotis O. i wsp.: Blood Pressure Reduction and Secondary Stroke Prevention: A Systematic Review and Metaregression Analysis of Randomized Clinical Trials. Hypertension 2017 Jan, 69(1): 171–179.
- Pires P.W., Dams Ramos C.M., Matin N., Dorrance A.M.: The effects of hypertension on the cerebral circulation. Am J Physiol Heart Circ Physiol 2013, 304: 1598–1614.
- PROGRESS Collaborative Group: Randomised trial of a perindopril- based blood-pressure-lowering regimen among 6,105 individuals with previous stroke or transient ischaemic attack. Lancet 2001, 358: 1033–1041.
- Dahlof B., Sever P.S., Poulter N.R. i wsp.: Prevention of cardiovascular events with an antihypertensive regimen of amlodipine adding perindopril as required versus atenolol adding bendroflumethiazide as required, in the Anglo-Scandinavian Cardiac Outcomes Trial-Blood Pressure Lowering Arm (ASCOT-BPLA): a multicentre randomised controlled trial. Lancet 2005, 366: 895–906.