
prof. dr hab. n. med. Adrian Doroszko
Krajobraz po burzy, czyli leczenie ozdrowieńca z wielochorobowością po COVID-19
Artykuł opublikowany w miesięczniku TERAPIA 2/2021
SUMMARY
The prolonged and longer-term observation of convalescents, extending with the pandemic’s duration, demonstrates that COVID-19, but also an asymptomatic or scarcely symptomatic course of SARS-CoV-2 infection, may initiate a chronic inflammatory process leading to degenerative changes in the cardiovascular, respiratory or central nervous systems. Changes initiated during the infection accelerate the course of coexisting chronic disorders, while the systemic immune response to the pathogen, including a cytokine storm leading to SIRS, initiates multiorgan changes that, if overlooked, may worsen the prognosis. Therefore, when taking care of a convalescent, one should not “automatically” return to all therapeutic regimens but optimize them, taking into consideration all the possible complications. Therefore, a thorough cardiological, pulmonological, neurological and endocrine assessment of a patient with multiple diseases should be performed and repeated regularly every couple to several months, to prevent a medical mistakes due to omission and so as not to overlook the beginning of life-threatening target complications. This brief review paper summarizes the current state of knowledge on the impact of a history of SARS-CoV-2 infection on the course of cardiovascular diseases, the pulmonary and endocrine system, and abnormalities. New chronic diseases initiated by the infection are also specified, since their overlooking can cost a patient’s life.
Keywords: COVID-19, convalescent, hypertension, chronic coronary syndrome, diabetes mellitus, congestive heart failure.
Słowa kluczowe: COVID-19, ozdrowieniec, nadciśnienie tętnicze, przewlekły zespół wieńcowy, cukrzyca, niewydolność serca.
Minął właśnie rok...
odkąd ludzkość stanęła oko w oko z jednym z największych zagrożeń w skali globalnej, jakim stał się wybuch pandemii SARS-CoV-2. Jeden rok intensywnie nabywanych doświadczeń z nową jednostką chorobową, której jako lekarze uczymy się z pokorą, często stając bezradnie w obliczu poniesionej porażki, ujawnił nam dane epidemiologiczne, pozwalające oszacować śmiertelność mieszczącą się w zakresie 3% w populacji ogólnej. Oznacza to, że 97% osób zdoła przeżyć infekcję, co ‒ niestety ‒ nie znaczy, że wrócą one do pełni zdrowia. Wydłużający się w miarę trwania pandemii okres obserwacji prospektywnej ozdrowieńców wskazuje jednoznacznie, że COVID-19, a niekiedy także bezobjawowy lub skąpoobjawowy przebieg infekcji SARS-CoV-2 mogą inicjować przewlekły proces zapalny, prowadząc do nieodwracalnych zmian degeneracyjnych w zakresie układu oddechowego, sercowo-naczyniowego czy ośrodkowego układu nerwowego (OUN). Choroby przewlekłe, współistniejące jeszcze przed wystąpieniem zakażenia, także mogą zmienić swój przebieg kliniczny, ulegając z reguły progresji do bardziej zaawansowanych stadiów, pogarszając tym samym znacząco rokowanie odległe.
Niniejsza praca w sposób syntetyczny podsumowuje aktualny stan wiedzy na temat wpływu przebytej infekcji SARS-CoV-2 na przebieg wybranych schorzeń układu sercowo-naczyniowego, oddechowego, wewnątrzwydzielniczego, ponadto wyszczególnione są możliwe nowe schorzenia przewlekle zainicjowane przez infekcję, których przeoczenie może kosztować życie pacjenta. Omawiany jest również sposób optymalnego podejścia do ozdrowieńca z wielochorobowością, u którego bezdyskusyjnie należy zoptymalizować terapię chorób przewlekłych, gdyż dotychczasowy schemat terapeutyczny może być zupełnie nietrafiony.
Nadciśnienie tętnicze
Wstępne wyniki badań eksperymentalnych uzyskane na początku pandemii wzbudziły spory niepokój. Sugerowały bowiem, że powszechnie stosowane inhibitory konwertazy angiotensyny (angiotensin-converting enzyme inhibitors, ACE-I) i blokery receptora 1 dla angiotensyny II (angiotensin receptor blockers, ARB, sartany) większają ekspresję izoformy 2 konwertazy angiotensyny ‒ ACE2 ‒ mogąc ułatwiać zakażenie narządu docelowego i sprzyjać progresji choroby.
Z drugiej strony, stosowanie ACE-I i ARB w kilku badaniach klinicznych było związane z mniejszą częstością występowania pozaszpitalnego zapalenia płuc w porównaniu z blokerami kanału wapniowego w kanadyjskiej kohorcie osób z nadciśnieniem tętniczym (1), a także ciężkości jego przebiegu, obejmującego konieczność hospitalizacji oraz zgon (2).
Badanie populacyjne ponad tysiąca przypadków COVID-19 z Madrytu z kilkunastotysięczną grupą kontrolną (1139 przypadków dodatnich/11 390 populacja kontrolna) wykazało, że inhibitory układu renina-angiotensyna-aldosteron (RAA) nie zwiększają odsetka chorych z COVID-19 wymagających hospitalizacji, w tym zgonów i przyjęć do oddziałów intensywnej terapii (OIT) (3). Także badanie ponad 6 tys. chorych z regionu Lombardii potwierdziło, że ACE-I i ARB nie wpływają na podatność na zakażenie, a także brak związku ciężkości i ostatecznego przebiegu zakażenia z faktem stosowania ACE-I lub ARB (4). Kolejne potwierdzenie uzyskano w przypadku grupy ponad 12 tys. przetestowanych pacjentów z Nowego Jorku, wykazując brak związku ACE-I i ARB z wynikiem testu (podatność) i ciężkością przebiegu zakażenia (5). Z kolei inne badanie wykazało, że w przypadku występowania nadciśnienia tętniczego stosowanie w terapii ACE-I/ARB przekładało się na redukcję śmiertelności z 9,8% w grupie nieleczonej blokerami układu RAA do 3,7% w przypadku stosowania ACE-I lub ARB (6).
Biorąc zatem pod uwagę fakt, iż powikłania sercowo-naczyniowe stanowią jeden z bardziej istotnych czynników ryzyka zgonu w przebiegu COVID-19 i okresie rekonwalescencji, utrzymanie leczenia nadciśnienia tętniczego z zastosowaniem ACE-I lub sartanów w okresie infekcji SARS-CoV-2, jako leków o korzystnym znaczeniu rokowniczym lub szybki powrót do takiej terapii po krótkotrwałej przerwie w okresie hospitalizacji mogą być kluczowe w redukcji częstości zdarzeń i śmiertelności w długotrwałej obserwacji. Obawy o niekorzystny wpływ sartanów na COVID-19 nie potwierdziły się i błędem medycznym, zwiększającym ryzyko powikłań i zgonu sercowo-naczyniowego, byłoby ich rutynowe odstawianie u chorych ze stwierdzonym zakażeniem SARS-CoV-2.
Pewnym problemem jest tendencja do hipotonii utrzymująca się po hospitalizacji, zwłaszcza w przypadkach o cięższym przebiegu, uniemożliwiająca powrót do wcześniejszej terapii. Jej dłuższe utrzymywanie się, mimo uprzedniej optymalizacji bilansu wodno-elektrolitowego i gospodarki kwasowo-zasadowej, wymaga zawsze pogłębienia diagnostyki, w tym uwzględnienia możliwości uszkodzenia nadnerczy w ostrej fazie choroby w przebiegu zespołu wykrzepiania wewnątrznaczyniowego (disseminated intravascular coagulation, DIC), o czym szerzej wspomniano w dalszej części niniejszego opracowania.
Zatorowość płucna
Stwierdzono jednoznacznie, że COVID-19 wiąże się ze zwiększoną aktywacją kaskady krzepnięcia (7), a dysfunkcja śródbłonka związana z niedotlenieniem może sprzyjać wykrzepianiu wewnątrznaczyniowemu podczas zakażenia. Badania pośmiertne wykazały zmiany w naczyniach płucnych, masywne zwłóknienie śródmiąższowe płuc, różne stopnie krwotocznego zawału płucnego, ciężkie uszkodzenie śródbłonka, rozległą zakrzepicę naczyniową z prawie całkowitym zamknięciem naczyń włosowatych pęcherzyków płucnych, strukturalnie zdeformowane naczynia włosowate i wzrost nowych naczyń poprzez mechanizmy neoangiogenezy (8). Ponadto rozsiane wykrzepianie wewnątrznaczyniowe (DIC) może być końcowym, letalnym zdarzeniem w ciężkim COVID-19 (9), a leczenie przeciwzakrzepowe wydaje się znacząco poprawiać rokowanie (10). Z tej perspektywy istotne jest wczesne rozpoznawanie incydentu zakrzepowo-zatorowego, szybkie włączenie leczenia przeciwkrzepliwego (low-molecular-weight heparin [LMWH]/novel oral anticoagulants [NOAC]) i utrzymanie go (NOAC) w okresie rekonwalescencji zgodnie z wytycznymi postępowania w zatorowości płucnej – przez przynajmniej 3 miesiące (zakładając, że COVID-19 był zidentyfikowanym przejściowym czynnikiem ryzyka), z opcją wydłużenia terapii zależnie od oceny kardiologicznej.
Choroba wieńcowa
COVID-19, podobnie jak każda infekcja, może w nieswoisty sposób zaostrzyć objawy przewlekłego zespołu wieńcowego, wtórnie z powodu hipoksemii w przypadku zapalenia płuc i towarzyszącego mu zwiększonego zapotrzebowania na tlen przez serce w przebiegu gorączki i ogólnoustrojowej reakcji zapalnej, zaburzeń równowagi elektrolitowej lub z powodu działań niepożądanych leków, takich jak stosowane na początku pandemii hydroksychlorochina i azytromycyna (11). U pacjentów z zaawanasowaną chorobą wieńcową brak rezerwy wieńcowej przy chorobie wielonaczyniowej może skutkować zwyżką troponin, dynamiką zmian ST-T i w konsekwencji niekiedy zawałem serca NSTEMI typu 2. W rzadszych przypadkach, wskutek ogólnoustrojowej reakcji zapalnej, może dojść do destabilizacji blaszki miażdżycowej i jej pęknięcia, prowadząc do okluzji tętnicy wieńcowej i wystąpienia STEMI. O ile druga sytuacja nie nastręcza wątpliwości diagnostyczno-terapeutycznych i standardy postępowania są tożsame jak u pacjentów bez COVID-19, o tyle niewielka zwyżka troponin przy słabo wyrażonych lub trudnych do zobiektywizowania z uwagi na stan pacjenta dolegliwościach stenokardialnych i jedynie dyskretnych zmianach ST-T może wzbudzać wątpliwości co do zasadności diagnostyki i leczenia interwencyjnego. Dlatego też w ostrym okresie infekcji podejście do takich pacjentów powinno być mocno zindywidualizowane, a celem stratyfikacji ryzyka i ułatwienia decyzyjności można posiłkować się skalą GRACE obowiązującą u chorych z NSTEMI (12). Należy pamiętać, że wzrost troponiny powyżej punktu odcięcia dla zakresu referencyjnego wskazywać może na nieswoiste uszkodzenie kardiomiocytów, m.in. wskutek procesu zapalnego (obecnie nie można wykluczyć, że SARS-CoV-2 może indukować zapalenie mięśnia serca o podostrym lub przewlekłym przebiegu; piorunujące nie należy do typowego obrazu choroby). Napady tachyarytmii, tachykardia wskutek reakcji zapalnej i gorączki, dysfunkcja nerek współistniejąca z zaburzeniami bilansu wodno-elektrolitowego również mogą nieswoiście przyczynić się do wzrostu troponiny.
Jednocześnie możemy mieć pewne trudności diagnostyczne u ozdrowieńca, który stwierdził spadek tolerancji wysiłku fizycznego lub pojawienie się bólów w klatce piersiowej, zaliczanych do nieswoistych objawów tzw. zespołu post-COVID. W każdej takiej sytuacji, szczególnie gdy u pacjenta występowała uprzednio choroba układu sercowo-naczyniowa lub jej podwyższone ryzyko, a także gdy w zapisie EKG pojawiają się niewidoczne uprzednio cechy martwicy lub zmiany ST-T, należy przeprowadzić rozszerzoną diagnostykę kardiologiczną, rozpoczynając od echokardiografii i w dalszej kolejności dedykowanej zależnie od prawdopodobieństwa metody diagnostyki choroby wieńcowej. Przejawem wtórnego zajęcia serca w COVID-19 może być też kardiomiopatia wywołana stresem‒ takotsubo (13).
Równocześnie należy dążyć do optymalizacji terapii u ozdrowieńca ze spółistniejącym rozpoznanym przewlekłym zespołem wieńcowym (14), pamiętając, że lekami o znaczeniu rokowniczym są kwas acetylosalicylowy (bądź klopidogrel w razie nietolerancji) oraz statyny w monoterapii lub w połączeniu z ezetimibem. Leczenie hipolipemizujące, jeśli zostało przerwane, trzeba włączyć niezwłocznie po potwierdzeniu prawidłowej funkcji wątroby. Leczenie przeciwdławicowe należy prowadzić zależnie od wartości ciśnienia tętniczego i tętna pacjenta (dokonując wyboru między β-blokerami – lekami preferowanymi, bezwzględnie wskazanymi po przebytym zawale mięśnia sercowego i/lub przy obniżonej frakcji wyrzutowej lewej komory a antagonistami wapnia jako dwiema grupami leków I rzutu, natomiast w II rzucie – trimetazydyną, iwabradyną, nitratami, ranolazyną lub nikorandilem). U pacjenta ze współistniejącym nadciśnieniem tętniczym warto rozważyć zastosowanie nebiwololu jako β-blokera o unikalnym działaniu wazodylatacyjnym, obniżającego ciśnienie centralne w aorcie, a więc obciążenie następcze dla lewej komory, a także – poprzez poprawę biodostępności tlenku azotu – wywierającego naczyniorozszerzające działanie także w wieńcowym łożysku naczyniowym. Antagoniści wapnia z grupy pochodnych dihydropirydyny, podobnie jak β-blokery, są obecnie preferowane jako leki przeciwdławicowe, w stosunku do nitratów, które obecnie powoli przechodzą do historii w leczeniu przewlekłym. Wybierając dihydropirydynowego antagonistę wapnia w terapii dławicy warto sięgnąć po leki nowszej generacji, które wolne są od typowych działań niepożądanych, jakimi są obrzęki obwodowe lub nasilona odruchowa tachykardia mogąca wtórnie nasilać niedokrwienie mięśnia serca. Rozsądnym wyborem w obrebie tej grupy leków może być zatem lerkanidypina. Jeśli tylko brak przeciwwskazań, każdy chory z przewlekłym zespołem wieńcowym i współistniejącą cukrzycą lub nadciśnieniem tętniczym powinien także otrzymać ACE-I lub ARB, i do takiego schematu terapeutycznego należy dążyć możliwie najszybciej w celu minimalizacji odległych powikłań COVID-19, jakimi są incydenty sercowo-naczyniowe.
Niewydolność serca
COVID-19 może być przyczyną dekompensacji uprzednio rozpoznanej i optymalnie leczonej przewlekłej niewydolności serca przyczyniając się do progresji choroby i pogarszając rokowanie odległe, natomiast współistniejąca niewydolność serca jest jednym z głównych czynników ryzyka ciężkiego przebiegu COVID-19 i wysokiej śmiertelności.
Spadek tolerancji wysiłku fizycznego i duszność wysiłkowa to objawy dość często obserwowane u ozdrowieńców. Jeśli jednak trwają one kilka‒kilkanaście tygodni, a zwłaszcza gdy pojawiają się inne objawy sugerujące możliwą dekompensację niewydolności serca (m.in. obrzęki obwodowe, cechy zastoju nad płucami), to należy niezwłocznie wdrożyć diagnostykę kardiologiczną, uwzględniając badanie echokardiograficzne i ocenę peptydów natriuretycznych. Po potwierdzeniu rozpoznania niewydolności serca należy systematycznie optymalizować dawkowanie leków, zgodnie z wytycznymi (15), dążąc do maksymalnych dawek docelowych lub największych tolerowanych przez pacjenta. Obecnie, z uwagi na relatywnie krótki czas trwania pandemii, trudno jest jednoznacznie określić odległe rokowanie w jednostce chorobowej, którą dopiero poznajemy. Nie można wykluczyć tropizmu wirusa do kardiomiocytów i inicjowania przewlekłego procesu zapalnego w mięśniu sercowym, prowadzącego w obserwacji wieloletniej do rozwoju kardiomiopatii i niewydolności serca. Dlatego, mimo braku jednoznacznych rekomendacji, rozsądne wydaje się utrzymanie racjonalnie wyważonego ambulatoryjnego nadzoru kardiologicznego nad ozdrowieńcami, obejmującego okresową kontrolę echokardiograficzną i skrining w kierunku zaburzeń rytmu i przewodzenia.
POChP i astma
Badania obserwacyjne w sposób mało zaskakujący i dość jednoznacznie wskazują, iż w porównaniu z pacjentami, którzy zachorowali na COVID-19 bez przewlekłej obturacyjnej choroby płuc, osoby z POChP miały bardziej nasiloną duszność i hipoksemię, większe nieprawidłowości w badaniach laboratoryjnych, obrazowych, co przekładało się na większe ryzyko przyjęcia na OIT (ok. 54%), wentylacji mechanicznej i zgonu (20%) (16). Tłumaczone jest to wyjściowym uszkodzeniem płuc, pozbawiającym je rezerw czynnościowych wobec wystąpienia ARDS (acute respiratory distress syndrome, zespół ostrej niewydolności oddechowej), co z kolei skutkuje znacznym postępem zmian w miąższu płuc i w efekcie progresją POChP u ozdrowieńca. W wielu badaniach odnotowano zwiększone ryzyko incydentów sercowo-naczyniowych u pacjentów z ostrym zaostrzeniem POChP, które zwłaszcza w ciągu pierwszych 30 dni może występować także w przebiegu COVID-19. Dlatego, oprócz zwracania większej uwagi na leczenie osób z POChP i COVID-19 w trakcie hospitalizacji, ważna jest również ich obserwacja w okresie kilkutygodniowej rehabilitacji w celu dalszego zmniejszenia śmiertelności, tym razem sercowo-naczyniowej.
Kluczowa jest tu optymalizacja schematów terapeutycznych współistniejących chorób układu krążenia (m.in. przewlekła niewydolność serca, przewlekły zespół wieńcowy, nadciśnienie tętnicze, cukrzyca, zaburzenia gospodarki lipidowej) – wczesne uzyskanie kontroli nad czynnikami ryzyka może znacząco zmniejszyć częstość incydentów sercowo-naczyniowych w tej szczególnej grupie chorych. Warto zauważyć, że spojrzenie na β-blokery u pacjentów ze współistniejącymi chorobami płuc uległo w ostatnich latach znaczącej zmianie. Istnieją dowody, że stosowanie tych leków ze wskazań kardiologicznych u chorych ze współistniejącą POChP zmniejsza częstość i ciężkość zaostrzeń. Niedawno również GINA (Global Initiative for Asthma – Światowa Inicjatywa na rzecz Zwalczania Astmy) zliberalizowała podejście do β-blokerów u pacjentów ze współistniejącą astmą – nie są one już bezwzględnie przeciwwskazane, a ich stosowanie należy rozważyć, jeśli korzyści sercowo-naczyniowe potencjalnie przewyższą stratę wynikającą z ewentualnego, aczkolwiek nie obserwowanego zbyt często, pogorszenia kontroli astmy. W obu sytuacjach – zarówno w przypadku astmy, jak i POChP, decydując się na wybór β-blokera, należy preferować leki wysoce kardioselektywne, jak na przykład nebiwolol.
Nieco inne obserwacje związane z zakażeniem SARS-CoV-2 dotyczą chorych ze współistniejącą astmą oskrzelową. Astma nie wiązała się ze zwiększonym ryzykiem hospitalizacji. Podobnie, stosowanie wziewnych kortykosteroidów z kortykosteroidami ogólnoustrojowymi lub bez nich nie wiązało się z hospitalizacją wynikającą z COVID-19 w okresie ostrych objawów zakażenia (17), choć według niektórych badań wziewna steroidoterapia może odgrywać pewną rolę ochronną przed ciężkim przebiegiem (18). Hipoteza ta wydaje się poparta badaniami in vitro dokumentującymi skuteczność samej steroidoterapii wziewnej lub w połączeniu z lekami rozszerzającymi oskrzela w hamowaniu replikacji koronawirusa i produkcji cytokin, a także dowodami in vivo (19). Co ciekawe, wykazano, że u chorych na astmę leczonych wziewnie glikokortykoidami występuje zmniejszona ekspresja ACE2 i transbłonowej proteazy seryny 2 (TMPRSS2) w plwocinie, którą uważa się za „kluczowego gracza” w procesie fuzji wirusa z błoną komórkową (20,21).
Pewne aspekty samej odpowiedzi immunologicznej typu 2, w tym cytokiny typu 2 (IL-4, IL-13 itp.), akumulacja eozynofilów, mogą zapewnić potencjalne działanie ochronne przeciwko COVID-19. Także immunoterapia alergenowa (allergen immunotherapy, AIT) i przeciwciało monoklonalne anty-IgE mogą zmniejszać ryzyko zakażenia wirusem w przypadku astmy poprzez łagodzenie stanu zapalnego lub wzmacnianie obrony przeciwwirusowej. Interakcje między COVID-19 a astmą zasługują na dalszą uwagę i wyjaśnienie. Infekcja SARS-CoV-2 może wiązać się z wystąpieniem zaostrzenia astmy, trwającego nadal po wyeliminowaniu wirusa, jednakże leczenie powinno być w tym przypadku typowe, zgodne z rekomendacjami GINA, bez nadmiernych obaw o działania niepożądane leków i ich ewentualną szkodliwość wobec zmienionych strukturalnie płuc na skutek przebytej infekcji.
Powikłania hormonalne
Badania autopsyjne pacjentów zmarłych z powodu COVID-19 wykazały, że tarczyca, przytarczyce, przysadka mózgowa, wewnątrzwydzielnicza część trzustki, a zwłaszcza nadnercza i jądra mogą ulegać uszkodzeniu na drodze różnorodnych mechanizmów (m.in. bezpośrednie uszkodzenie przez SARS-CoV-2, wskutek zapalnej odpowiedzi immunologicznej, zaburzeń naczyniowych – mikrozatorowości oraz indukowanych w okresie zakażenia reakcji autoimmunologicznych). Kilka obserwacyjnych badań klinicznych potwierdziło przyżyciowo czynnościowe zaburzenia endokrynologiczne (22).
Nadnercza
Na podstawie aktualnych danych nie ma dowodów, iż pacjenci z niewydolnością nadnerczy są narażeni na zwiększone ryzyko zarażenia COVID-19. Wiadomo jednak, że osoby z niedoczynnością kory nadnerczy, jak i z wrodzonym przerostem nadnerczy mają nieco zwiększone ogólne ryzyko infekcji. Ponadto pierwotna niedoczynność kory nadnerczy jest związana z upośledzeniem funkcji odporności naturalnej, z wadliwym działaniem neutrofilów i komórek NK (natural killer) (8). Może to częściowo wyjaśniać ten nieznacznie zwiększony wskaźnik chorób zakaźnych u tych pacjentów, a także ogólną zwiększoną śmiertelność. To ostatnie można również tłumaczyć niewystarczającym kompensacyjnym zwiększeniem dawki hydrokortyzonu na początku epizodu infekcji. Z tych wszystkich powodów osoby z niewydolnością kory nadnerczy mogą być bardziej narażone na powikłania medyczne i ostatecznie zwiększone ryzyko śmiertelności w przypadku COVID-19. Jak dotąd nie ma jednoznacznych doniesień dotyczących wyników zakażenia COVID-19 u pacjentów z niewydolnością kory nadnerczy. Przy podejrzeniu COVID-19 w przypadku pojawienia się drobnych objawów należy niezwłocznie i bez obaw o ewentualną immunosupresję wprowadzić modyfikację leczenia zastępczego, co oznacza w pierwszej kolejności co najmniej podwojenie zwykłych dawek zastępczych glikokortykoidów, aby uniknąć przełomu nadnerczowego.
W opublikowanych dotychczas pracach nie udowodniono jednoznacznie możliwości bezpośredniej agresji wirusa na nadnercza u wcześniej zdrowych osób (23,24). Posocznice wirusowa, bakteryjna i grzybicza mogą powodować krwotok, martwicę lub zakrzepicę na poziomie nadnerczy, a w konsekwencji ostrą niedoczynność kory nadnerczy. Co więcej, ostatnie odkrycia wskazują na ryzyko wystąpienia żylnej choroby zakrzepowo-zatorowej u chorych na COVID-19, a u niektórych z nich na korzystne leczenie heparyną (25). Dlatego należy wziąć pod uwagę, że ostra niewydolność nadnerczy może być również spowodowana zdarzeniem zakrzepowym na poziomie nadnerczy u pacjentów z COVID-19. Konsekwencją tego może być ostra niewydolność kory nadnerczy z upośledzoną produkcją hormonów, a następnie wstrząs i pogorszenie możliwości reakcji na ciężką niewydolność oddechową. Wykonywanie w odpowiednim czasie badań przesiewowych pod kątem czynności osi przysadka-nadnercza i identyfikacja tego stanu pozwala na zastosowanie odpowiedniej terapii zastępczej, która pomaga uniknąć silnego wstrząsu. Obserwowana niekiedy w ostrej fazie COVID-19 hipotonia słabo reagująca na aminy katecholowe oraz pojawiająca się bez innej przyczyny hiponatremia z hiperkaliemią, niebędące wyrazem SIADH (syndrome of inappropriate antidiuretic hormone hypersecretion, zespół niewłaściwego uwalniania wazopresyny), mogą pośrednio na to wskazywać. Iluzoryczna poprawa kontroli ciśnienia tętniczego po przebytej infekcji, skutkująca tendencją do hipotonii mimo zaprzestania stosowania leków, może też być wtórna do uszkodzenia nadnerczy i ich względnej niedomogi, nie oznaczając tym samym skutecznego wyleczenia choroby nadciśnieniowej, a jedynie wskazując na możliwość zagrażającej życiu niedoczynności nadnerczy. Szczegółowa ocena endokrynologiczna w takich przypadkach jest kluczowa w ocenie funkcji nadnerczy i w efekcie odległego rokowania.
Cukrzyca
Diabetycy z COVID-19 są bardziej narażeni na gorsze rokowanie i śmiertelność. Otyłość i cukrzyca charakteryzują się przewlekłym stanem zapalnym o niskim stopniu nasilenia ze zwiększonym stężeniem prozapalnej leptyny i zmniejszonym uwalnianiem przeciwzapalnej adiponektyny. Ponadto osoby z otyłością są często nieaktywne fizycznie, bardziej oporne na insulinę i mają dysbakteriozę jelit, co może nasilać reakcję zapalną w odpowiedzi na zakażenie SARS-CoV-2. Prawdopodobieństwo wystąpienia burzy cytokinowej jest większe u osób z cukrzycą, co więcej, w przypadku wysokiego miana wirusa, zdolność do wywołania ostrej odpowiedzi immunologicznej może być upośledzona u tych pacjentów, narażając ich na cięższe działania niepożądane. Ponadto osoby z otyłością mają niższe stężenia witaminy D (26), co również może osłabić odpowiedź immunologiczną, jakkolwiek dokładna rola suplementacji jest obecnie oceniana w trwających badaniach klinicznych. Cukrzyca jest związana ze stanem prozakrzepowym, z brakiem równowagi między czynnikami krzepnięcia a fibrynolizą oraz ze zwiększonym ryzykiem zdarzeń zakrzepowozatorowych. Wstępne raporty dotyczące przebiegu zakażenia koronawirusem dotyczyły głównie osób z cukrzycą typu 2, chociaż ostatnie badania wykazały, że także pacjenci z cukrzycą typu 1 są narażeni na ciężki COVID-19. Natomiast cukrzyca per se nie zwiększa podatności na wystąpienie zakażenia koronawirusem. Co istotne, pewne leki przeciwcukrzycowe i leki przeciwwirusowe mogą w pewnym zakresie modulować ryzyko zgonu, ale należy dokładnie ocenić ograniczenia ich stosowania i potencjalne interakcje z testowanymi swoistymi terapiami COVID-19 (tab. 1).
Dotychczasową terapię przeciwcukrzycową można kontynuować u pacjentów leczonych w szpitalu przy regularnym przyjmowaniu kalorii i płynów w zależności od stanu klinicznego, ryzyka wystąpienia działań niepożądanych leku i interakcji między lekami przeciwcukrzycowymi a preparatami stosowanymi w leczeniu COVID-19. Jednak insulina jest preferowanym środkiem kontroli glikemii u chorych na cukrzycę leczonych w szpitalu, a jej stosowanie jest obowiązkowe u osób w stanie krytycznym.
Glikokortykoidy podawane u pacjentów z COVID-19 z zespołem ostrej niewydolności oddechowej jako leczenie objawowe i przeciwzapalne mogą pogłębić insulinooporność, podtrzymać glukoneogenezę, pogorszyć kontrolę glikemii i spowodować wyraźną hiperglikemię, a także – przez zakłócanie działania GLP-1 (glucagon-like peptide 1) – zwiększanie produkcji glukagonu.
Objawy ostrej infekcji w przebiegu zakażenia koronawirusem mogą stanowić czynnik pogarszający kontrolę cukrzycy wywołać ostre powikłania metaboliczne poprzez bezpośredni negatywny wpływ na czynność komórek β. Wpływ ten może też powodować cukrzycową kwasicę ketonową u osób z cukrzycą, hiperglikemię przy przyjęciu do szpitala u pacjentów bez cukrzycy w wywiadzie i potencjalnie nową cukrzycą (27). Po wypisie, w okresie rekonwalescencji konieczna jest rewizja stosowanych leków, z preferowanym powrotem do skojarzenia preparatów o znaczeniu rokowniczym w redukcji częstości zdarzeń sercowo-naczyniowych (metformina, inhibitory SGLT-2 i analogi GLP-1), uwzględniając pozostałe, w tym insulinoterapię jako opcję uzupełniającą przy braku uzyskania kontroli glikemii ww. lekami. Wskutek zaburzeń metabolicznych zachodzących w okresie ostrej infekcji i ubytku masy ciała może dojść do zmiany zapotrzebowania na leki przeciwcukrzycowe, zaś powrót „na ślepo” do dawkowania sprzed choroby wiąże się z ryzykiem hipoglikemii.
Tabela 1. Leczenie cukrzycy w ostrej fazie COVID-19 (27)
| Grupa leków przeciwcukrzycowych | Zalety | Wady | Interakcje z terapią CO VID -19 |
|---|---|---|---|
| Metformina | Brak ryzyka hipoglikemii | Ryzyko kwasicy mleczanowej w przebiegu ARDS, ciężkiego uszkodzenia nerek lub zaawansowanej niewydolności serca | Lopinawir |
| Inhibitory DPP-4 (dipeptidyl peptidase 4, „gliptyny”) | Brak ryzyka hipoglikemii Możliwość stosowania w przypadku szerokiego zakresu dysfunkcji nerek Potencjalne działanie przeciwzapalne Potencjalna modyfikacja wiązania SARS-CoV-2 z DPP-4 | Brak | Lopinawir/Ritonawir Atazanawir |
| Inhibitory SGL T-2 (sodium-glucose co-transporter 2, „flozyny”) | Brak ryzyka hipoglikemii | Ryzyko hipowolemii Zaburzenia elektrolitowe Euglikemiczna kwasica ketonowa | Lopinawir/Ritonawir |
| Agoniści receptora GL P-1 | Brak ryzyka hipoglikemii Potencjalne działanie przeciwzapalne | Ryzyko objawów niepożądanych ze strony przewodu pokarmowego | Atazanawir |
| Pochodne sulfonylomocznika | Brak | Ryzyko hipoglikemii, zwłaszcza przy równoległym stosowaniu innych leków przeciwcukrzycowych | Lopinawir/Ritonawir Hydroksychlorochina |
| Pioglitazon | Działanie przeciwzapalne | Ryzyko retencji płynów i niewydolności serca | Fawipirawir |
| Insulina | Zalecana u ciężko chorych pacjentów | Ryzyko hipoglikemii Potrzeba podaży parenteralnej | Hydroksychlorochina |
Zaburzenia erekcji i ryzyko uszkodzenia gonad
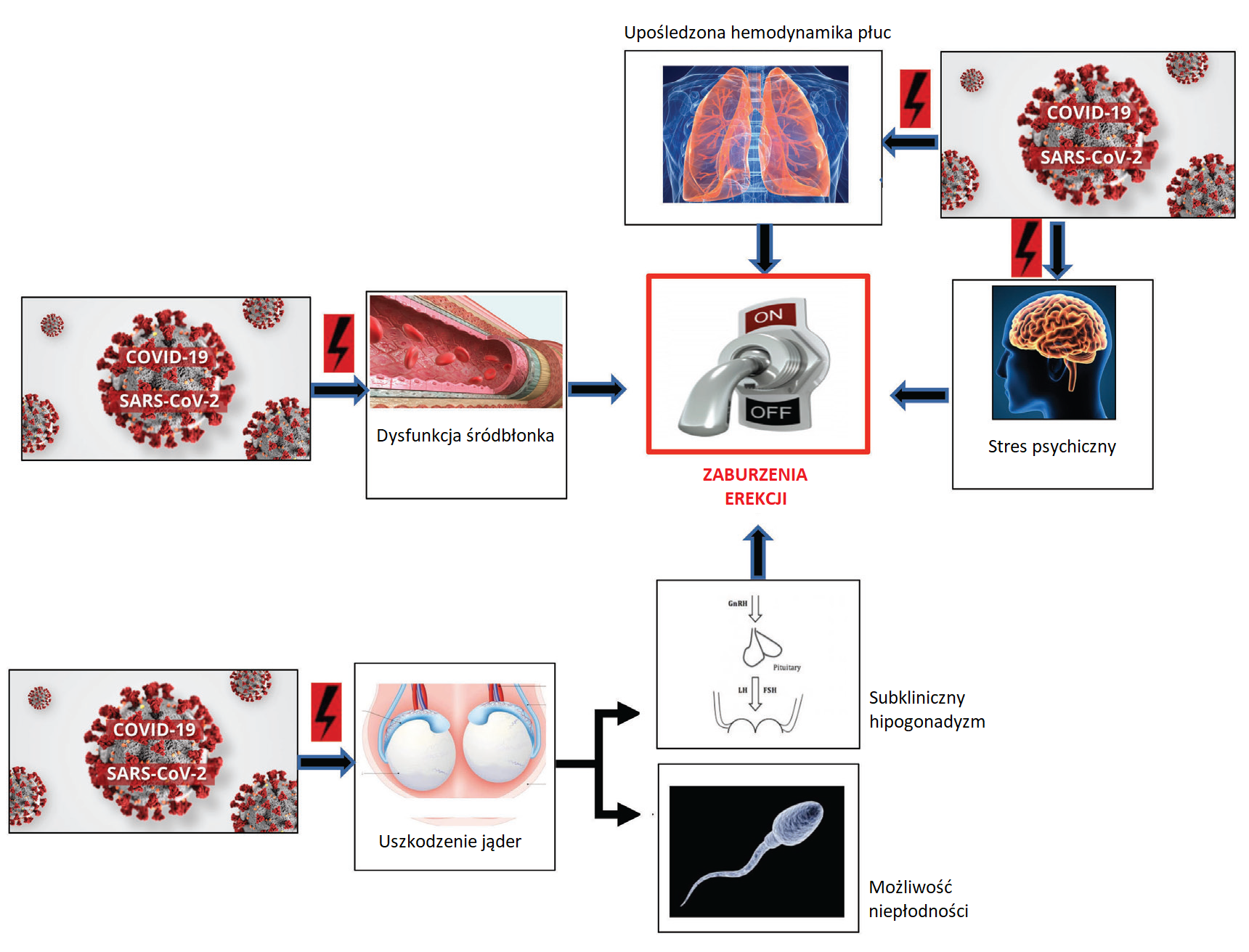
Dysfunkcja śródbłonka, subkliniczny hipogonadyzm, stres psychiczny i upośledzona hemodynamika płuc – wszystko to przyczynia się do potencjalnego wystąpienia zaburzeń erekcji (ryc. 1). Ponadto COVID-19 może inicjować lub zaostrzyć przebieg uprzednio istniejących chorób sercowo-naczyniowych, co dodatkowo zwiększa ich ryzyko.
Czynność jąder u pacjentów z COVID-19 wymaga dokładnego zbadania pod kątem niejasnego związku z niedoborem testosteronu i możliwymi konsekwencjami dla zdrowia reprodukcyjnego, mogąc wpływać po przebytej infekcji na samą jakość nasienia i w efekcie na płodność. Pewne obawy budzi także ryzyko uszkodzenia jąder w wyniku zakażenia COVID-19. W rzeczywistości ACE2 ulega silnej ekspresji w jądrach, co sugeruje możliwość zakażenia jąder już od wczesnego stadium choroby (28). Obecna zarówno w komórkach Sertolego, jak i Leydiga (29) izoforma 2 konwertazy angiotensyny odgrywa kluczową rolę w spermatogenezie i regulacji steroidogenezy. Ze względu na zaangażowanie komórek Sertolego funkcje rozrodcze mogą być podobnie dotknięte. Dodatkowo ACE2 jest również obecna w spermatogoniach, co zwiększa ryzyko obecności SARS-CoV-2 w płynie nasiennym (30).
Pojawienie się zaburzeń erekcji jako zastępczego markera zdrowia sercowo-naczyniowego może również stać się przydatną, szybką i niedrogą metodą pierwszego rzutu oceny powikłań płucnych i sercowo-naczyniowych u osób, które przeżyły COVID-19. W tym względzie pomocne są wyniki procedur diagnostycznych, jak ultrasonografia dopplerowska czy ocena osi podwzgórze-przysadka-gonady.
Oceniając potencjalne przyczyny wystąpienia zaburzeń erekcji, szczególnie u pacjenta ze współistniejącym nadciśnieniem tętniczym, warto zwrócić uwagę na stosowany schemat terapii hipotensyjnej i go ewentualnie zoptymalizować. Warto zauważyć, że β-blokery o małej kardioselektywności (jak np. atenolol o niemal historycznym znaczeniu lub metoprolol preferowany u chorych z zaburzeniami rytmu), a także diuretyki tiazydowe, poza niekorzystnym działaniem metabolicznym promującym rozwój zaburzeń gospodarki lipidowej i sprzyjającym rozwojowi cukrzycy, mogą wtórnie wywoływać zaburzenia erekcji. W tym kontekście warto zoptymalizować terapię na metabolicznie neutralną, co wtórnie może także zniwelować objawy dysfunkcji seksualnej – spośród β-blokerów warto rozważyć stosowanie nebiwololu, diuretyki tiazydowe zamienić na tiazydopodobne, albo – jeśli pacjent nie ma do tendencji do obrzęków – zamiast diuretyków zastosować antagonistów wapnia nowej generacji, jak np. lerkanidypinę.
Co istotne, zaburzeniom erekcji, szczególnie u młodszych pacjentów, może być początkowo mylnie przypisywana etiologia wyłącznie psychogenna, wynikająca z długotrwałego stresu towarzyszącego pandemii, długotrwałej izolacji, ze społeczno-ekonomicznych skutków choroby dla pacjenta, które w konsekwencji długoterminowo pozbawiają go komfortu życia. Dokonując swoistego bilansu zdrowia u pacjenta po COVID-19, należy zwrócić uwagę na możliwość występowania zaburzeń erekcji, zbierając szczegółowy wywiad w tym zakresie, a w razie potwierdzenia ‒ konsultować go przede wszystkim kardiologicznie i endokrynologiczne. Dopiero po wykluczeniu tła somatycznego powinno rozważyć się psychoterapię niwelującą psychiczne skutki przebytej infekcji i pandemii.
Rycina 1. Powiązanie zaburzeń erekcji u chorych po przebytym COVID-19 z możliwym uszkodzeniem układu sercowo-naczyniowego, oddechowego, wewnątrzwydzielniczego oraz zdrowia psychicznego
Tarczyca
Hormony tarczycy koordynują i regulują główne szlaki metaboliczne i biochemiczne. ACE2, która ułatwia wejście SARS-CoV-2 do komórki gospodarza za pomocą białka kolczastego, ulega wzmożonej ekspresji u osób z nieprawidłową funkcją tarczycy, co z kolei może nasilać ryzyko i ciężkość przebiegu infekcji SARS-CoV-2. Zwrócono uwagę na rolę hamowania ACE2 przez SARS-CoV-2 jako ważny aspekt przebiegu COVID-19 (31), a odnotowana nadmierna reakcja immunologiczna uważana jest przez niektórych badaczy bardziej za konsekwencję pierwotnie upośledzonej ścieżki endokrynnej niż za bezpośrednią odpowiedź na sam patogen (32). Nie można wykluczyć możliwej lokalizacji SARS-CoV-2 na poziomie tarczycy.
Tyreotoksykoza w przebiegu COVID-19, rozwijająca się m.in. wskutek zapalenia tarczycy, może pogorszyć przebieg schorzeń sercowo-naczyniowych, prowadząc m.in. do tachyarytmii. Dlatego szybka ocena wolnych hormonów tarczycy i TSH pozwala na wczesne rozpoznanie i odpowiednią terapię oraz pomaga uniknąć poważniejszych powikłań. O ile podostre zapalenie tarczycy często pojawia się kilka tygodni po zakażeniu wirusowym górnych dróg oddechowych i może być późnym powikłaniem zakażenia SARS-CoV-2 (a jednym z jego objawów jest ból w okolicy szyi i uszu), o tyle czynność tarczycy należy monitorować również w okresie obserwacji chorych na COVID-19. W przypadku obecności podostrego zapalenia tarczycy lub niedoczynności nadnerczy leczenie kortykosteroidami powinno być obowiązkowe w celu zastąpienia czynności nadnerczy, unikając w ten sposób niebezpiecznego pogorszenia stanu klinicznego tych pacjentów (33).
Obecnie nie ma dostępnych danych, które sugerowałyby, że chorzy z autoimmunologicznym zapaleniem tarczycy są narażeni na większe ryzyko COVID-19 i wydaje się prawdopodobne, że większość pacjentów bezobjawowych i łagodnie dotkniętych powinna być leczona tak jak zwykle. Chociaż ryzyko związane z lekami przeciwtarczycowymi, a ściślej z immunosupresją wynikającą z neutropenii polekowej pozostaje, prawdopodobnie nie jest bezpośrednio związane z takimi pacjentami, którzy powinni być leczeni w zwykły sposób. U osób z COVID-19 o ciężkim przebiegu zmiany w czynności tarczycy mogą wiązać się z zespołem niskiej fT3 i fT4 (euthyroid sick syndrome, ESS), a w dalszej kolejności mogą wystąpić zmiany strukturalne i czynnościowe w tarczycy oraz w obrębie pozostałych składowych osi podwzgórze-przysadka-tarczyca, których diagnostyka u ozdrowieńców wymaga wnikliwej prospektywnej obserwacji.
Pierwsza konsultacja ozdrowieńca – czas na rewizję leczenia
COVID-19 u osoby z wielochorobowością powoduje poważne zachwianie homeostazy ustroju, uderzając w narządy, które zdrowotnie stanowią „pietę achillesową” chorego i były przedmiotem leczenia jeszcze przed infekcją. Ogólnoustrojowa odpowiedź zapalna stanowi swoisty twardy reset dla organizmu, odsłaniając najsłabsze ogniwa i dekompensując narządy z wyjściowo naruszonymi rezerwami czynnościowymi, a także inicjuje wiele nowych powikłań i chorób przewlekłych. Oceniając zatem dobrostan pacjenta po przebytym zakażeniu, w sposób oczywisty w pierwszej kolejności powinniśmy się skoncentrować na optymalizacji terapii i ocenie progresji dotychczasowych chorób przewlekłych, mając na uwadze możliwe nowe powikłania, które początkowo w stadium subklinicznym mogą być trudno uchwytne. Każdy pacjent z wielochorobowością wymaga zatem wnikliwej analizy, ze szczególnym uwzględnieniem oceny kardiologicznej, pulmonologicznej, neurologicznej i endokrynologicznej, zanim rozpoznamy restitutio ad integrum. Często powrót do poprzedniego leczenia może nie dawać optymalnych rezultatów – np. tendencja do hipotonii lub utrzymywanie się zaburzeń elektrolitowych mogą uniemożliwić szybki powrót do optymalnej terapii przewlekłej niewydolności serca, przebyte zmiany zapalne w płucach mogą uczynić dotychczasową terapię POChP niewystarczającą, a znaczny ubytek masy ciała w przebiegu infekcji skutkuje hipoglikemią polekową u chorego z cukrzycą.
Z kolei pacjentów dotychczas zdrowych należy wyczulić na potencjalne powikłania odległe, wskazując ich możliwe spektrum oraz zakres rzeczowy badań mających na celu ich racjonalną diagnostykę. Warto zauważyć, że przedłużający się zespół przewlekłego zmęczenia, nieustępujący spadek tolerancji wysiłku fizycznego, duszność wysiłkowa czy pojawienie się de novo zaburzeń erekcji u dotychczas zdrowego pacjenta mogą wskazywać na uszkodzenie układu sercowo-naczyniowego i powinny budzić niepokój oraz być powodem do przeprowadzenia szczegółowych badań.
Podsumowanie
Przeżycie COVID-19 przez pacjenta z wielochorobowością, wobec braku swoistej terapii przeciwwirusowej, stanowi swoisty prezent od losu, ale z licznymi rysami. Zapoczątkowane w okresie zakażenia zmiany znacząco destabilizują przebieg już istniejących chorób przewlekłych, a przebyta ogólnoustrojowa odpowiedź immunologiczna na patogen, przybierająca niekiedy postać burzy cytokinowej prowadzącej do wystąpienia SIRS (systemic inflammatory response syndrome, zespół ogólnoustrojowej reakcji zapalnej), inicjuje zmiany wielonarządowe, które przeoczone mogą znacząco pogorszyć rokowanie odległe. Dlatego, przejmując opiekę nad ozdrowieńcem, nie należy „automatycznie” wracać do wszystkich schematów terapeutycznych stosowanych przed infekcją, a optymalizować je, uwzględniając pojawiające się możliwe powikłania. Należy zatem dokonać dokładnej, powtarzanej cyklicznie co kilka‒kilkanaście miesięcy oceny kardiologicznej, pulmonologicznej, neurologicznej i endokrynologicznej pacjenta z wielochorobowością, by nie popełnić błędu medycznego z zaniechania ani przeoczyć rozpoczynających się, zagrażających życiu powikłań odległych. Rolą lekarza rodzinnego jest więc zarówno uświadomienie pacjentowi, że przebycie COVID-19 może być sukcesem połowiczym i należy rozpocząć okresowe przeglądy stanu zdrowia, jak i wskazanie zasadności poszczególnych konsultacji oraz koordynacja ich zakresu rzeczowego i ram czasowych.
Piśmiennictwo:
- Shah S., McArthur E., Farag A. i wsp.: Risk of hospitalization for community acquired pneumonia with renin–angiotensin blockade in elderly patients: a population-based study. PLoS One 2014, 9: e110165.
- Kang J.H., Kao L.T., Lin H.C. i wsp.: Do outpatient statins and ACEIs/ARBs have synergistic effects in reducing the risk of pneumonia? A population-based case-control study. PLoS One 2018, 13: e0199981.
- de Abajo F.J., Rodríguez-Martín S., Lerma V. i wsp.; MED-ACE2-COVID19 study group: Use of renin-angiotensin-aldosterone system inhibitors and risk of COVID-19 requiring admission to hospital: a case-population study. Lancet 2020, 395(10238):1705–1714.
- Mancia G., Mancia G., Rea F. i wsp.: Renin-Angiotensin-Aldosterone System Blockers and the Risk of Covid-19. N Engl J Med 2020, 382(25): 2431–2440.
- Reynolds H.R., Adhikari S., Pulgarin C. i wsp.: Renin-Angiotensin-Aldosterone System Inhibitors and Risk of Covid-19. N Engl J Med 2020, 382(25): 2441–2448.
- Zhang P., Zhu L., Cai J. i wsp.: Association of Inpatient Use of Angiotensin-Converting Enzyme Inhibitors and Angiotensin II Receptor Blockers with Mortality Among Patients With Hypertension Hospitalized With COVID-19. Circ Res 2020 Jun 5, 126(12): 1671–1681.
- Tang N., Li D., Wang X., Sun Z.: Abnormal coagulation parameters are associated with poor prognosis in patients with novel coronavirus pneumonia. J Thromb Haemost 2020, 18:844–847.
- Ackermann M., Verleden S.E., Kuehnel M. i wsp.: Pulmonary vascular endothelialitis, thrombosis, and angiogenesis in Covid-19. N Engl J Med 2020 Jul 9, 383(2): 120‒128.
- McGonagle D., O’Donnell J.S., Sharif K. i wsp.: Immune mechanisms of pulmonary intravascular coagulopathy in COVID-19 pneumonia. Lancet Rheumatol 2020, 2: e437–e445.
- Tang N., Bai H., Chen X. i wsp.: Anticoagulant treatment is associated with decreased mortality in severe coronavirus disease 2019 patients with coagulopathy. J Thromb Haemost 2020, 18:1094–1099.
- Babapoor-Farrokhran S., Gill D., Walker J. i wsp.: A Myocardial injury and COVID-19: possible mechanisms. Life Sci 2020 Jul 15, 253: 117723.
- Collet J.P., Thiele H., Barbato E. i wsp.; ESC Scientific Document Group: 2020 ESC Guidelines for the management of acute coronary syndromes in patients presenting without persistent ST-segment elevation. Eur Heart J 2020 Aug 29: ehaa575. Doi:10.1093/eurheartj/ehaa575. [Epub ahead of print]
- Sala S., Peretto G., Gramegna M. i wsp.: Acute myocarditis presenting
as a reverse Tako-Tsubo syndrome in a patient with SARS-CoV-2 respiratory infection. Eur Heart J 2020, 41: 1861–1862. - Knuuti J., Wijns W., Saraste A. i wsp.; ESC Scientific Document Group 2019: ESC Guidelines for the diagnosis and management of chronic coronary syndromes. Eur Heart J 2020 Jan 14, 41(3): 407–477.
- Ponikowski P., Voors A.A., Anker S.D. i wsp.; ESC Scientific Document Group: 2016 ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure: The Task Force for the diagnosis and treatment of acute and chronic heart failure of the European Society of Cardiology (ESC)Developed with the special contribution of the Heart Failure Association (HFA) of the ESC. Eur Heart J 2016 Jul 14, 37(27): 2129–2200.
- Wu F., Zhou Y., Wang Z. i wsp.; Medical Treatment Expert Group for COPD and COVID-19: Clinical characteristics of COVID-19 infection in chronic obstructive pulmonary disease: a multicenter, retrospective, observational study. J Thorac Dis 2020 May, 12(5): 1811–1823.
- Chhiba K.D., Patel G.B., Vu T.H.T. i wsp.: Prevalence and characterization of asthma in hospitalized and nonhospitalized patients
with COVID-19. J Allergy Clin Immunol 2020 Aug, 146(2): 307–314.e4. - Rogliani P., Lauro D., Di Daniele N. i wsp.: Reduced risk of COVID- 19 hospitalization in asthmatic and COPD patients: a benefit of inhaled corticosteroids? Expert Rev Respir Med 2020 Dec 3: 1–8. Doi: 10.1080/17476348.2021.1850275. [Epub ahead of print]
- Yamaya M., Nishimura H., Deng X. i wsp.: Inhibitory effects of glycopyrronium, formoterol, and budesonide on coronavirus HCoV-229E replication and cytokine production by primary cultures of human nasal and tracheal epithelial cells. Respiratory Invest 2020, 58(3): 155–168.
- Hoffmann M., Kleine-Weber H., Schroeder S. i wsp.: SARSCoV-2 cell entry depends on ACE2 and TMPRSS2 and is blocked by a clinically proven protease inhibitor. Cell 2020, 181(2): 271–280.e8.
- Peters M.C., Sajuthi S., Deford P. i wsp.: COVID-19 related genes in sputum cells in Asthma: relationship to demographic features and corticosteroids. Am J Respir Crit Care Med 2020, 202(1): 83–90.
- Parolin M., Parisotto M., Zanchetta F. i wsp.: Coronaviruses and Endocrine System: a Systematic Review on Evidences and Shadows. Endocr Metab Immune Disord Drug Targets 2020 Sep 5. Doi: 10.21 74/1871530320666200905123332. [Epub ahead of print]
- Porfidia A., Pola R., Porfidia A. i wsp.: Venous thromboembolism in COVID-19 patients. J Throm Haemost 2020 Jun, 18(6): 1516‒1517.
- Isidori A.M., Arnaldi G., Boscaro M. i wsp.: COVID-19 infection and glucocorticoids: update from the Italian Society of Endocrinology Expert Opinion on steroid replacement in adrenal insufficiency. J Endocrinol Invest 2020 Aug, 43(8): 1141‒1147.
- Scaroni C., Armigliato M., Cannavò S.: COVID-19 outbreak and steroids administration: are patients treated for Sars-Cov-2 at risk of adrenal insufficiency? J Endocrinol Invest 2020 Jul, 43(7): 1035‒1036.
- Mitchell F.: Vitamin-D and COVID-19: do deficient risk a poorer outcome? Lancet Diabetes Endocrinol 2020, 8: 570.
- Apicella M., Campopiano M.C., Mantuano M. i wsp.: COVID-19 in people with diabetes: understanding the reasons for worse outcomes. Lancet Diabetes Endocrinol 2020 Sep, 8(9): 782–792. Erratum in: Lancet Diabetes Endocrinol 2020 Oct, 8(10): e5. Erratum in: Lancet Diabetes Endocrinol 2020 Nov, 8(11): e6.
- Younis J.S., Abassi Z., Skorecki K.: Is there an impact of the COVID-19 pandemic on male fertility? The ACE2 connection. Am J Physiol Endocrinol Metab 2020, 318(6): E878–E880.
- Douglas G.C., O’Bryan M.K., Hedger M.P. i wsp.: The novel angiotensin-converting enzyme (ACE) homolog, ACE2, is selectively expressed by adult Leydig cells of the testis. Endocrinology 2004, 145(10): 4703–4711.
- Wang Z., Xu X.: scRNA-seq profiling of human testes reveals the presence of the ACE2 receptor, a target for SARS-CoV-2 infection in spermatogonia Leydig and Sertoli. Cells 2020, 9: 4.
- Verdecchia P., Cavallini C., Spanevello A., Angeli F.: The pivotal link between ACE2 deficiency and SARS-CoV-2 infection. Eur J Intern Med 2020 Jun, 76: 14–20.
- Grassi T., Varotto E., Galassi F.M.: COVID-19, a viral endocrinological disease? Eur J Intern Med 2020 Jul, 77: 156–157.
- Bellastella G., Maiorino M.I., Esposito K.: Endocrine complications of COVID-19: what happens to the thyroid and adrenal glands? J Endocrinol Invest 2020 Aug, 43(8): 1169–1170.